최신개정법령
최신개정법령
화장품의 색소 종류와 기준 및 시험방법 [별표 3]
- 작성자: py러닝메이트
- 작성일: 2021.01.13
- 조회수: 835
[별표 3]
통칙 및 일반시험법
Ⅰ. 통칙
1. 「알루미늄레이크」란 알루미늄이 결합하여 흡착시킨 색소를 말한다.
2. 각 색소의 화학명에 분자식 및 분자량을 표기한다.
3. 별표 1의 색소 중 별표 2에서 규정하지 않은 기준 및 시험방법의 경우 과학적·합리적으로 타당성이 인정되는 자사 기준 및 시험방법을 설정하여 시험할 수 있다.
4. 이 기준에서 규정하지 않는 정의, 시험법 등은 「대한민국약전」(식품의약품안전처 고시)의 통칙, 일반시험법, 제제총칙, 「기능성화장품 기준 및 시험방법(식품의약품안전처 고시) 및 의약외품에 관한 기준 및 시험방법(식품의약품안전처 고시) 등의 규정에 따라 판정한다.
Ⅱ. 일반시험법
1. 가용물시험법
2. 강열잔분시험법
3. 건조감량 및 강열감량시험법
4. 기체크로마토그래프법
5. 납시험법
6. 레이크시험법
7. 물가용물시험법
8. 미생물한도시험법
9. 박층크로마토그래프법
10. 불꽃반응시험법
11. 불소시험법
12. 불용물시험법
13. 비소시험법
14. 비중측정법
15. 산가용물시험법
16. 산불용물시험법
17. 색소시험법
18. 수은시험법
19. 염색반응시험법
20. 염화물시험법
21. 원자흡광광도법
22. 유도결합플라즈마발광광도법
23. 융점측정법
24. 자외가시부흡광도측정법
25. 적외부스펙트럼측정법
26. 정량법
27. 정성반응
28. 중금속시험법
29. 질소정량법
30. 철시험법
31. 황산염시험법
32. 회분시험법
33. 흡광도측정법
34. pH측정법
35. 시약・시액・표준액・용량분석용 표준액・박층크로마토그래프용 표준품・계량기・용기
1. 가용물시험법
가용물시험법은 검체 중에 함유되어 있는 물 또는 유기용매에 녹을 수 있는 물질의 양을 시험하는 방법으로 그 양을 질량백분율 (%)로 나타낸다.
장 치 다음 중 어느 한쪽의 추출기를 이용한다.
1) 속슬레추출기
2) 공통으로 사용할 수 있는 연속추출기
그림 1. 속슬레추출기의 예 그림 2. 공통으로 사용할 수 있는 연속추출기의 예
조 작 법
제 1 법 검체 약 5g을 원통 여과지에 정밀하게 달아 추출용이소프로필에텔 100 mL를 넣고 속슬레추출기에서 2 시간 추출한다. 미리 질량을 알고 있는 증발접시에 추출액을 옮기고 추출기를 추출용이소프로필에텔 10 mL로 씻은 다음 씻은 액을 증발접시에 합한다. 이것을 수욕에서 가열하여 추출용이소프로필에텔을 날려보내고 데시케이터(실리카겔)에서 항량이 될 때까지 건조한 다음 그 질량(W1)을 정밀하게 단다. 다음 원통여과지의 추출잔류물에 추출용이소프로필에텔 100 mL를 넣고 속슬레추출기에서 2 시간 추출한다. 미리 질량을 알고 있는 증발접시에 추출액을 옮기고 추출기를 추출용이소프로필에텔 10 mL로 씻은 다음 씻은 액을 증발접시에 합한다. 이것을 수욕에서 가열하여 추출용이소프로필에텔를 날려보내고 데시케이터(실리카겔)에서 항량이 될 때까지 건조한 다음 그 질량(W2)을 정밀하게 달아 다음 식에 따라 이소프로필에텔 추출분을 구한다.
제 2 법 중성에텔 추출분, 알카리성에텔 추출분 및 산성에텔 추출분을 각각 구하여 이것의 총합을 에텔 추출분 (%)으로 한다.
1) 중성에텔 추출분
검체 약 5 g을 정밀하게 달아 물 200 mL를 넣어 녹이고 분액깔대기에 옮긴다. 추출용이소프로필에텔 100 mL를 넣어 1 분간 잘 흔들어 섞고 가만히 방치한 다음 이소프로필에텔층을 취하고 이 조작을 3 회 반복한다. 이 조작에서 얻은 추출액을 합하고 물층은 따로 보존한다. 추출에 사용한 분액깔대기를 추출용이소프로필에텔 10 mL를 넣어 씻고 씻은 액을 여액에 합한다. 이 액에 물 20 mL를 넣고 잘 섞은 다음 씻는 조작을 세액에 색깔이 나타나지 않을 때까지 반복하고 세액은 따로 보존한다. 이 조작에서 얻은 이소프로필에텔층을 플라스크에 옮기고 이것에 분액깔대기를 추출용이소프로필에텔 10 mL로 씻은 다음 씻은 액을 합한다. 이것을 증류하여 증발ㆍ농축하고 약 50 mL로 한 다음 미리 질량을 알고 있는 증발접시에 옮기고, 이것에 플라스크를 추출용이소프로필에텔 10 mL로 씻은 다음, 씻은 액을 합한다. 이것을 온탕의 수욕에서 가만히 두고 가온하여 건조하고 데시케이터(실리카겔)에서 항량이 될 때까지 건조한 다음, 질량을 정밀하게 달고, 다음 식에 따라 중성에텔 추출분을 구한다.
2) 알칼리성에텔 추출분
1)에서 따로 보존한 물층에 따로 보존한 씻은 액을 합하고, 이것에 수산화나트륨용액(1 → 10)2 mL를 넣고, 분액깔대기에 옮긴다. 추출용이소프로필에텔 100 mL를 넣고 1 분간 잘 흔들어 섞고, 가만히 놓아둔 다음 이소프로필에텔층을 취하는 조작을 3 회 반복한다. 이 조작에서 얻은 추출액을 합하고, 물층은 따로 보존한다. 추출에 사용한 분액깔대기를 추출용이소프로필에텔 10 mL를 넣어 씻고, 씻은 액을 여액에 합한다. 이것에 묽은수산화나트륨시액 20 mL를 넣고 잘 섞은 다음 씻는 조작을 세액에 색깔이 나타나지 않을 때까지 반복하고, 세액은 따로 보존한다. 이 조작에서 얻은 이소프로필에텔층을 플라스크에 옮기고, 이것에 분액깔대기를 추출용이소프로필에텔 10 mL로 씻은 다음, 씻은 액을 합한다. 이것을 제거하고, 약 50 mL로 한 다음, 미리 질량을 알고 있는 증발접시에 옮기고, 이것에 플라스크를 추출용이소프로필에텔 10 mL로 씻은 다음, 씻은 액을 합한다. 이것을 온탕의 수욕에서 가만히 두고 가온하여 건조하고, 데시케이터(실리카겔)에서 항량이 될 때까지 건조한 다음, 질량을 정밀하게 달고, 다음 식에 따라 알칼리성에텔 추출분을 구한다.
3) 산성에텔 추출분
2)에서 따로 보존한 물층에 따로 보존한 씻은 액을 합하고, 이것에 묽은염산(1 → 2) 3 mL를 넣고, 분액깔대기에 옮긴다. 추출용이소프로필에텔 100 mL를 넣고 1 분간 잘 흔들어 섞고, 가만히 놓아둔 다음 이소프로필에텔층을 취하는 조작을 3 회 반복한다. 이 조작에서 얻은 추출액을 합하고, 이것에 추출에 이용한 분액깔대기를 추출용이소프로필에텔 10 mL로 씻은 다음, 씻은 액을 합한다. 이것에 묽은염산(1 → 200) 20 mL를 넣고 잘 섞은 다음 씻는 조작을 물층에 색깔이 나타나지 않을 때까지 반복한다. 이 조작에서 얻은 이소프로필에텔층을 플라스크에 옮기고, 이것에 분액깔대기를 추출용이소프로필에텔 10 mL로 씻은 다음, 씻은 액을 합한다. 이것을 증류하여 증발ㆍ농축하고, 약 50 mL로 한 다음, 미리 질량을 알고 있는 증발접시에 옮기고, 이것에 플라스크를 추출용이소프로필에텔 10 mL로 씻은 다음, 씻은 액을 합한다. 이것을 온탕의 수욕에서 가만히 두고 가온하여 건조하고, 데시케이터(실리카겔)에서 항량이 될 때까지 건조한 다음, 질량을 정밀하게 달고, 다음 식에 따라 산성에텔 추출분을 구한다.
제 3 법 중성에텔 추출분, 알칼리성에텔 추출분 및 산성에텔 추출분 중, 규격으로 규정한 추출분의 합으로써 에텔 추출분이라고 한다.
1) 중성에텔 추출분
검체 약 5g을 정밀하게 달아, 물 100 mL를 넣어 녹이고, 공통으로 사용할 수 있는 연속추출기의 추출기 A로 추출한다. 따로 플라스크 B에 추출용이소프로필에텔 100 mL를 넣고, 온탕의 수욕에서 가온하면서, 5 시간 추출한다. 이 조작에서 얻은 추출액을 합하고, 이것을 분액깔대기로 옮긴 다음, 물층은 따로 보존한다. 추출에 사용한 플라스크 B를 추출용이소프로필에텔 10 mL로 씻은 다음, 씻은 액을 추출액에 합한다. 이것에 물 20 mL를 넣고, 잘 섞은 다음 씻는 조작을 세액에 색깔이 나타나지 않을 때까지 반복하고, 세액은 따로 보존한다. 이 조작에서 얻은 이소프로필에텔층을 플라스크에 옮기고, 이것에 분액깔대기를 추출용이소프로필에텔 10 mL로 씻은 다음, 씻은 액을 합한다. 이것을 증류하여 증발ㆍ농축하고, 약 50 mL로 한 다음, 미리 질량을 알고 있는 증발접시에 옮기고, 이것에 플라스크를 추출용이소프로필에텔 10 mL로 씻은 다음, 씻은 액을 합하고, 온탕의 수욕에서 가만히 두고 가온하여 건조하고, 데시케이터(실리카겔)에서 항량이 될 때까지 건조한 다음, 질량을 정밀하게 달고, 제 2 법의 1)에 있는 식에 따라 중성에텔 추출분을 구한다.
2) 알칼리성에텔 추출분
1)의 추출기 A의 수용액에 수산화나트륨용액(1 → 10) 2 mL를 넣고 추출한다. 따로 플라스크 B에 추출용이소프로필에텔 100 mL를 넣고, 온탕의 수욕에서 가온하면서, 5 시간 추출한다. 이 조작에서 얻은 추출액을 합하고, 이것을 분액깔대기로 옮긴 다음, 물층은 따로 보존한다. 추출에 사용한 플라스크 B를 추출용이소프로필에텔 10 mL로 씻은 다음, 씻은 액을 추출액에 합한다. 이것에 묽은수산화나트륨시액 20 mL를 넣고 잘 섞은 다음 씻는 조작을 물층에 색깔이 나타나지 않을 때까지 반복하고, 세액은 따로 보존한다. 이 조작에서 얻은 이소프로필에텔층을 플라스크에 옮기고, 이것에 분액깔대기를 추출용이소프로필에텔 10 mL로 씻은 다음, 씻은 액을 합한다. 이것을 제거하고, 약 50 mL로 한 다음, 미리 질량을 알고 있는 증발접시에 옮기고, 이것에 플라스크를 추출용이소프로필에텔 10 mL로 씻은 다음, 씻은 액을 합한다. 이것을 온탕의 수욕에서 가만히 두고 가온하여 건조하고, 데시케이터(실리카겔)에서 항량이 될 때까지 건조한 다음, 질량을 정밀하게 달고, 제 2 법의 2)에 있는 식에 따라 알칼리성에텔 추출분을 구한다.
3) 산성에텔 추출분
2)의 추출기 A의 수용액에 묽은염산(1 → 2)3 mL를 넣고 추출한다. 따로 플라스크 B에 추출용이소프로필에텔 100 mL를 넣고, 온탕의 수욕에서 가온하면서, 5 시간 추출한다. 이 조작에서 얻은 추출액을 합하고, 이것을 분액깔대기로 옮긴 다음, 이것에 플라스크 B를 추출용이소프로필에텔 10 mL로 씻고, 씻은 액을 합한다. 이것에 묽은 염산(1 → 200) 20 mL를 넣고 잘 섞은 다음 씻는 조작을 물층에 색깔이 나타나지 않을 때까지 반복한다. 이 조작에서 얻은 이소프로필에텔층을 플라스크에 옮기고, 이것에 분액깔대기를 추출용이소프로필에텔 10 mL로 씻은 다음, 씻은 액을 합한다. 이것을 제거하고, 약 50 mL로 한 다음, 미리 질량을 알고 있는 증발접시에 옮기고, 이것에 플라스크를 추출용이소프로필에텔 10 mL로 씻은 다음, 씻은 액을 합한다. 이것을 온탕의 수욕에서 가만히 두고 가온하여 건조하고, 데시케이터(실리카겔)에서 항량이 될 때까지 건조한 다음, 질량을 정밀하게 달고, 제 2 법의 3)에 있는 식에 따라 산성에텔 추출분을 구한다.
제 4 법 검체 약 5 g을 정밀하게 달아, 묽은수산화나트륨용액(2 → 100) 100 mL를 넣어 녹이고, 공통으로 사용할 수 있는 연속추출기로 추출한다. 플라스크 B에 추출용이소프로필에텔 100 mL를 넣고, 온탕의 수욕에서 가온하면서, 5 시간 추출한다. 이 조작에서 얻은 추출액을 합하고, 이것을 분액깔대기로 옮긴 다음, 이것에 플라스크 B를 추출용이소프로필에텔 10 mL로 씻고, 씻은 액을 합한다. 여기에 묽은수산화나트륨시액 20 mL를 넣고 잘 섞은 다음 씻는 조작을 물층에 색깔이 나타나지 않을 때까지 반복한다. 이 조작에서 얻은 이소프로필에텔층을 플라스크에 옮기고, 이것에 분액깔대기를 추출용이소프로필에텔 10 mL로 씻은 다음, 씻은 액을 합한다. 이것을 제거하고, 약 50 mL로 한 다음, 미리 질량을 알고 있는 증발접시에 옮기고, 이것에 플라스크를 추출용이소프로필에텔 10 mL로 씻은 다음, 씻은 액을 합한다. 이것을 온탕의 수욕에서 가만히 두고 가온하여 건조하고, 데시케이터(실리카겔)에서 항량이 될 때까지 건조한 다음, 질량을 정밀하게 달고, 제 2 법의 2)에 있는 식에 따라 알칼리성에텔 추출분을 구한다.
제 5 법 검체 약 5 g을 원통여과지에 정밀하게 달아 아세톤 100 mL를 넣고 속슬레추출기에서 2 시간 추출한다. 미리 질량을 알고 있는 증발접시에 추출액을 옮기고 이것에 추출기를 아세톤 10 mL로 씻은 다음 씻은 액을 합한다. 아세톤을 날려 보내고, 데시케이터(실리카겔)에서 항량이 될 때까지 건조한 다음 그 질량(W1)을 정밀하게 단다. 그 다음 추출잔류물에 아세톤 100 mL를 넣고, 속슬레추출기에서 2 시간 추출한다. 미리 질량을 알고 있는 증발접시에 추출액을 옮기고, 이것에 추출기를 아세톤 10 mL로 씻은 다음, 씻은 액을 합한다. 아세톤을 제거하고 데시케이터(실리카겔)에서 항량이 될 때까지 건조한 다음, 그 질량(W2)을 정밀하게 달아 다음 식에 따라 아세톤 추출분을 구한다.
제 6 법 검체 약 5 g을 정밀하게 달아 물 약 190 mL를 넣고, 세게 흔들고 섞는다. 그 다음 2 시간에 걸쳐 흔들고 섞은 뒤, 물을 넣고 200 mL로 하고 여과지로 여과한다. 이 여액 100 mL를 미리 질량을 알고 있는 증발접시에 정확하게 달아, 수욕에서 건고한다. 이것을 105 ℃에서 항량이 될 때까지 건조하고, 데시케이터(황산)에서 실온이 될 때까지 방치하여 식힌 다음, 그 질량을 정밀하게 달아 다음 식에 따라 물 가용분을 구한다.
제 7 법 검체 약 5 g을 원통 여과지에 정밀하게 달아 클로로포름 100 mL를 넣고 속슬레추출기에서 6 시간 추출한다. 미리 질량을 알고 있는 증발접시에 추출액을 옮기고, 이것에 추출기를 클로로포름 30 mL로 씻은 다음 씻은 액을 합한다. 클로로포름을 날려 보내고 데시케이터(실리카겔)에서 항량이 될 때 까지 건조한 다음, 그 질량(W1)을 정밀하게 단다. 그 다음 추출잔류물에 클로로포름 100 mL를 넣고 속슬레추출기에서 6 시간 추출한다. 미리 질량을 알고 있는 증발접시에 추출액을 옮기고, 이것에 추출기를 클로로포름 30 mL로 씻은 다음, 씻은 액을 합한다. 클로로포름을 날려 보내고 데시케이터(실리카겔)에서 항량이 될 때까지 건조한 다음, 추출물의 질량(W2)을 정밀하게 달아 다음 식에 따라 클로로포름 추출분을 구한다.
2. 강열잔분시험법
강열잔분시험법은 검체를 다음 조작법에 따라 강열하였을 때 휘발하지 않고 남는 물질의 양을 측정하는 방법으로 검체 중에 함유되어 있는 무기물의 양을 시험하는 방법이다.
조 작 법 검체를 넣을 백금, 석영 또는 사기로 만든 도가니를 미리 항량이 될 때까지 강열하고 데시케이터(실리카겔)에서 방치하여 식힌 다음 그 질량을 정밀하게 단다. 검체는 약 1 g을 달아 앞의 용기에 넣고 그 질량을 정밀하게 단다. 여기에 황산 소량을 넣어 검체를 적시고 천천히 가열하여 될 수 있는 대로 낮은 온도에서 거의 회화 또는 휘산 시킨 다음 일단 방냉하고 다시 황산 소량을 넣어 검체를 적시고 천천히 가열하여 될 수 있는 대로 낮은 온도에서 항량이 될 때까지 강열한다. 방냉은 데시케이터 (실리카겔) 에서 실온이 될 때까지 식힌 다음 그 질량을 정밀하게 달고 그 질량 차를 잔분으로 하여 다음 식에 따라 강열잔분을 구한다.
3. 건조감량 및 강열감량시험법
건조감량 및 강열감량시험법은 검체를 건조 또는 강열할 때 손실되는 수분 및 기타의 휘발성물질의 양의 한도를 시험하는 방법이다.
가. 건조감량
검체가 큰 결정이나 덩어리일 때는 빨리 분쇄하여 지름 약 2mm 이하의 크기로 하고 따로 규정이 없는 한 그 1∼2g을 미리 검체의 건조조건에 따라 약 30분간 건조하여 무게를 단 평량병에 넣어 두께가 5mm 이하의 층이 되도록 편편하게 한 다음 정밀히 달고 이를 건조기에 넣어 마개를 열고 규정에 따라 건조한 다음 마개를 닫고 건조기에서 꺼내어 무게를 단다. 가열한 때에는 식힌 다음 평량한다. 검체가 규정의 건조온도보다 낮은 온도에서 녹을 때에는 그 녹는 온도보다 5∼10℃ 낮은 온도에서 1∼2시간 건조한 다음 규정의 온도에서 건조한다.
나. 강열감량
건조감량시험법에 따라 시험한다. 다만, 따로 규정이 없는 한 가열온도 450∼550℃로 하고, 평량병 대신 백금제, 석영제 또는 자제도가니를 쓴다.
4. 기체크로마토그래프법
기체크로마토그래프법은 적당한 고정상을 써서 만든 칼럼에 검체혼합물을 주입하고 이동상으로 불활성기체 (운반기체)를 써서 고정상에 대한 유지력의 차를 이용하여 각각의 성분으로 분리하여 분석하는 방법이다. 기체검체 또는 기화할 수 있는 검체에 적용할 수 있으며 물질의 확인, 순도시험, 정량 등에 쓴다. 칼럼에 주입된 혼합물은 각 성분이 고유한 비율 k로 이동상 및 고정상에 분포한다.
이 비율 k, 이동상의 칼럼통과시간 t0 (k = 0인 물질을 주입한 때부터 그 물질의 피크정점까지의 시간) 및 유지시간 tR (피검검체의 주입한 때부터 피검물질의 피크정점까지의 시간)과의 사이에는 다음과 같은 관계가 있으므로 같은 조건인 경우 유지시간은 물질의 고유한 값이 된다.
tR = (1 + k)t0
장 치 보통 운반기체도입부, 유량제어장치, 검체도입부, 칼럼, 칼럼항온조, 검출기 및 기록장치로 되어 있고 필요하면 연소기체, 조연(助燃)기체 및 부가(付加)기체 등의 도입장치, 유량제어장치, 헤드스페이스용검체도입장치 등을 쓴다. 운반기체도입부 및 유량제어장치는 운반기체를 일정한 유량으로 칼럼으로 보내는 것으로 보통 압력조절밸브, 유량조절밸브, 압력계 등으로 구성된다. 검체도입장치는 일정량의 검체를 정확하고 재현성이 좋게 운반기체 유로 중에 도입하기 위한 장치로 충전칼럼용과 모세관칼럼용이 있다. 또한 모세관칼럼용검체도입장치에는 분할도입방식과 비분할도입방식의 장치가 있다. 보통 칼럼은 충전칼럼 및 모세관칼럼의 두 종류가 있다. 충전칼럼은 일정한 크기의 기체크로마토그래프용충전제를 불활성인 금속, 유리 또는 합성수지의 관에 균일하게 충전한 것이다. 충전칼럼 중 안지름이 1 mm 이하의 것은 충전모세관칼럼 (마이크로팩트칼럼)이라고도 한다. 모세관칼럼은 불활성인 금속, 유리, 석영 또는 합성수지의 관 내면에 기체크로마토그래프용 고정상을 보유한 중공구조이다. 칼럼항온조는 필요한 길이의 칼럼을 수용할 수 있는 용적으로 칼럼온도를 일정하게 유지하기 위한 온도제어장치를 가지고 있다. 검출기는 칼럼에서 분리된 성분을 검출하는 것으로 알칼리열이온화검출기, 염광광도검출기, 질량분석계, 불꽃이온화검출기, 전자포획검출기, 열전도도검출기 등이 있다. 기록장치는 검출기에 의하여 얻어진 신호의 강도를 기록하는 것이다.
조 작 법 따로 규정이 없는 한 다음 방법에 따른다. 장치를 미리 조정한 다음 의약품각조에서 규정하는 조작조건의 검출기, 칼럼 및 운반기체를 써서 운반기체를 일정한 유량으로 흐르게 하고 칼럼을 규정 온도에서 평형이 되게 한 다음 의약품각조에서 규정하는 양의 검액 또는 표준액을 검체도입장치를 써서 주입한다. 분리된 성분은 검출기로 검출하여 기록장치에서 크로마토그램을 얻는다.
확인 및 순도시험 이 방법을 확인시험에 사용하는 경우 검액의 피검성분과 표준피검물질의 유지시간이 일치하는 것 또는 검액에 표준피검물질을 첨가하여도 피검물질의 피크 모양이 유지되는 것으로 확인시험을 한다. 이 방법을 순도시험에 사용하는 경우 보통 검액 중 혼재물의 한도에 대응하는 농도의 표준액을 쓰는 방법 또는 면적백분율법으로 시험한다. 따로 규정이 없는 한 검액의 이성체비는 면적백분율법으로 구한다. 면적백분율법은 크로마토그램에서 얻은 각 성분의 피크면적의 합계를 100으로 하고 이에 대한 각 성분의 피크면적비로부터 조성비를 구한다. 다만 정확한 조성비를 얻기 위해서는 혼재물의 주성분에 대한 감도계수에 의해 피크면적을 보정한다.
정 량 보통 내부표준법에 따르지만 적당한 내부표준물질을 얻을 수 없을 때에는 절대검량선법으로 시험한다. 정량결과에 대하여 피검물질 이외의 물질의 영향을 무시할 수 없을 경우에는 표준첨가법으로 시험한다 .
1) 내부표준법 내부표준법에서는 일반적으로 피검물질에 되도록 가까운 유지시간을 가지며 그 어느 피크와도 완전하게 분리되는 안정한 물질을 내부표준물질로 선택한다. 의약품각조에서 규정하는 내부표준물질 일정량에 표준피검물질을 단계적 농도가 되도록 넣어 여러 개의 표준액을 만든다. 이들 표준액 일정량씩을 주입하여 얻은 크로마토그램으로부터 내부표준물질의 피크면적 또는 피크높이에 대한 표준피검물질의 피크면적비 또는 피크높이비를 구한다. 이 비를 세로축으로 하고 표준피검물질의 양 또는 내부표준물질의 양에 대한 표준피검물질의 양의 비를 가로축으로 하여 검량선을 작성한다. 이 검량선은 보통 원점을 지나는 직선이 된다. 다음에 의약품각조에서 규정하는 방법으로 같은 양의 내부표준물질을 넣은 검액을 만들어 검량선을 작성하였을 때와 같은 조건으로 크로마토그램을 얻어 그 내부표준물질의 피크면적 또는 피크높이에 대한 피검물질의 피크면적 또는 피크높이의 비를 구하여 검량선을 써서 피검물질의 양을 구한다. 의약품각조에서는 보통 검량선이 직선이 되는 농도범위에 들어가는 한 개의 표준액 및 이 표준액의 농도에 가까운 농도의 검액을 만들어 의약품각조에서 규정하는 각각의 양을 주입한 다음 같은 조건으로 기체크로마토그래프법에 따라 시험하여 피검물질의 양을 구한다.
2) 절대검량선법 표준피검물질을 단계적 농도가 되도록 취하여 여러 개의 표준액을 만들고 표준액 일정량씩을 정확하고 재현성 있게 주입하여 크로마토그램을 얻는다. 얻어진 크로마토그램으로부터 표준피검물질의 피크면적 또는 피크높이를 세로축으로 하고 표준피검물질의 양을 가로축으로 하여 검량선을 작성한다. 이 검량선은 보통 원점을 지나는 직선이 된다. 다음에 의약품각조에서 규정하는 방법으로 검액을 만들어 검량선을 작성할 때와 같은 조건으로 크로마토그램을 얻어 피검물질의 피크면적 또는 피크높이을 구하고 검량선을 써서 피검물질의 양을 구한다. 의약품각조에서는 보통 검량선이 직선이 되는 농도범위에 들어가는 한 개의 표준액 및 이 표준액의 농도에 가까운 농도의 검액을 만들어 의약품각조에서 규정하는 각각의 양을 주입한 다음 같은 조건으로 기체크로마토그래프법에 따라 시험하여 피검물질의 양을 구한다. 이 방법은 모든 측정조작을 엄밀하게 일정한 조건으로 하여 시험한다.
3) 표준첨가법 4 개 이상의 일정한 양의 검액을 정확하게 취한다. 이 중 1 개를 제외한 나머지 검액에 피검물질의 표준액을 단계적 농도가 되도록 정확하게 넣는다. 이 액 및 먼저 제외한 1 개의 액을 각각 정확하게 일정량이 되도록 희석하여 각각 검액으로 한다. 이 액 일정량씩을 정확히 재현성있게 주입하여 얻어진 크로마토그램에서 각각의 피크면적 또는 피크높이를 구한다. 각각의 검액에 넣은 피검물질의 농도로부터 표준액 첨가에 의한 피검물질의 증가량을 구하여 가로축으로 하고 피크면적 또는 피크높이를 세로축으로 하여 관계선을 작성한다. 관계선의 가로축과의 교점과 원점 사이의 거리로부터 피검물질의 양을 구한다. 또한 이 방법은 절대검량선법으로 피검물질의 검량선을 작성하였을 때 검량선이 원점을 지나는 직선일 때 적용할 수 있다. 또 모든 측정조작을 엄밀하게 일정한 조건으로 하여 시험한다.
피크측정법 보통 다음 방법을 쓴다.
1) 피크높이측정법 가) 피크높이법 피크의 정점에서 기록지의 가로축으로 내린 수직선과 피크의 양끝을 연결하는 접선 (기저선)과의 교점으로부터 정점까지의 길이를 측정한다.
나) 자동피크높이법 검출기로부터의 신호를 데이터처리장치를 써서 피크높이를 측정한다.
2) 피크면적측정법 가) 반치폭법 피크높이의 1/2 위치에서의 피크폭에 피크높이를 곱한다.
나) 자동적분법 검출기로부터의 신호를 데이터처리장치를 써서 피크면적을 측정한다.
시스템적합성 시스템적합성은 크로마토그래프법을 이용하는 시험법에서 중요한 필수항목이며, 의약품의 시험에 이용하는 시스템이 해당시험을 수행하는데 적절한 성능을 가지는지 여부를 그 시스템을 사용하여 시험할 때마다 확인하기 위해 실시된다. 시스템적합성의 시험방법 및 판정기준은 의약품의 품질규격으로 설정한 시험법 중에 규정하여야 한다. 만약 규정된 판정기준을 충족하지 못한 경우에는 해당 시스템을 이용한 품질시험 결과는 인정하지 않는다.
시스템적합성은 「시스템의 성능」 및 「시스템의 재현성」 항으로 평가하며, 순도시험의 경우에는 「검출의 확인」 항도 평가하는 경우가 있다.
1) 검출의 확인 순도시험에서 대상으로 하는 유연물질 등의 피크가 그 규격한도값 수준의 농도에서 확실하게 검출되는 것을 확인함으로서 사용하는 시스템이 시험의 목적을 달성하기 위해 필요한 성능을 갖추고 있다는 것을 검증한다.
순도시험 중 정량시험의 경우 보통 「검출의 확인」 항을 설정하여 규격한도값 수준의 용액을 주입할 때의 반응의 폭을 규정하고 한도값 부근에서 반응이 직선성을 가진다는 것을 나타낸다. 한도시험과 같이 규격한도값과 같은 농도의 표준액을 써서 검액으로부터의 반응정도와 비교하여 시험하는 경우나 한도값 수준에서의 검출을 「시스템의 재현성」 등으로 확인할 수 있는 경우에는 「검출의 확인」 항은 설정하지 않아도 된다.
2) 시스템의 성능 피검성분에 대한 특이성이 확보되어 있음을 확인하는 것으로서 사용하는 시스템이 시험의 목적을 달성하기 위해 필요한 성능을 가진다는 것을 검증한다.
정량법에서는 원칙적으로 피검성분과 분리확인용 물질 (인접한 피크가 바람직하다)의 분리도 및 필요한 경우에 유출순서로 규정한다. 순도시험에서는 원칙적으로 피검성분과 분리확인용 물질 (인접한 피크가 바람직하다)의 분리도 및 유출순서로 규정한다. 또한 필요한 경우에는 대칭계수를 같이 규정한다. 다만 적당한 분리확인용 물질이 없는 경우에는 이론단수 및 대칭계수로 규정할 수 있다.
3) 시스템의 재현성 표준액 또는 시스템적합성용액을 반복하여 주입했을 때 대상성분의 측정값들의 정밀도가 시험의 목적에 적절한 수준인지를 확인하여 해당 시스템이 시험에 적합한 성능을 갖추고 있는지를 검증한다.
시스템의 재현성의 허용한도값은 보통 반복 주입하여 얻은 대상성분의 반응의 상대표준편차 (RSD)로 규정한다. 검액을 주입하기 전에 표준액의 주입을 반복하는 형태와 표준액을 검액의 주입 전과 후로 나누어 주입하는 형태 및 검액을 주입하는 사이사이에 표준액을 주입하는 형태로 시스템의 재현성을 확인할 수도 있다.
각 표준액 주입형태의 반복하여 주입하는 횟수는 6 회를 원칙으로 하나, 농도기울기법을 쓰는 경우나 검액 중에 유출이 느린 성분이 섞여 있는 경우 등 1 회 분석시간이 긴 경우에는 6 회 주입 때와 거의 동등한 시스템의 재현성이 확보되도록 정밀도의 허용한도값을 엄격하게 규정함으로서 반복 주입의 횟수를 줄일 수 있다.
시스템의 재현성의 허용한도값은 해당시험법의 적용을 검토한 자료와 시험에 필요한 정밀도 등을 고려하여 적절한 수준으로 설정한다.
조작조건의 변경에 관한 유의사항 의약품각조의 조작조건 중에서 칼럼의 안지름 및 길이, 충전제의 입자경, 고정상의 농도 또는 두께, 칼럼온도, 가온속도, 운반기체의 종류 및 유량, 분할비는 시스템적합성의 규정에 적합한 범위 내에서 일부 변경할 수 있다. 다만, 헤드스페이스용검체주입장치 및 그 조작조건은 규정하는 방법보다 더 좋은 정확도와 정밀도를 얻을 수 있는 범위 내에서 변경할 수 있다.
용 어
S/N 비 (Signal to Noise ratio) 다음의 식으로 정의한다.
H : 대상물질의 피크의 기저선 (노이즈의 중앙값)으로부터 피크높이
h : 검액 또는 공시험액 중 대상물질의 피크 주변의 크로마토그램의 노이즈의 폭
기저선 및 노이즈는 대상물질의 피크높이의 1/2 위치 피크폭의 20 배에 해당하는 범위에서 측정한다. 공시험액을 사용하는 경우에는 대상물질이 유출하는 위치 근처에서 위와 같은 범위에서 측정한다.
대칭계수 크로마토그램상의 피크의 대칭성의 정도를 나타내는 것으로 대칭계수 S로서 다음식으로 정의한다.
W0.05h : 피크의 기저선에서부터 피크높이의 1/20의 높이에서의 피크폭
f : W0.05h의 피크폭을 피크의 정점에서 기록지의 가로축에 내린 수직선으로 2 등분할 때의 피크의 올라가는 쪽의 거리
다만 W0.05h 및 f는 같은 단위를 쓴다.
상대표준편차 보통 다음식으로 정의되는 상대표준편차 (RSD) (%)로 규정한다.
: 측정값
: 측정값의 평균값
n : 측정회수
피크의 완전분리 피크가 완전분리된다는 것은 분리도 1.5 이상을 의미한다.
피크밸리비 크로마토그램 상의 두 피크 사이에서 기저선 분리가 얻어지지 못하는 경우에 해당 피크들 사이의 분리의 정도를 표시한다. 피크밸리비 p/v는 다음의 식으로 정의한다.
Hp : 크로마토그램의 작은 피크의 기저선으로부터의 피크높이
Hv : 크로마토그램의 큰 피크와 작은 피크 사이의 가장 낮은 지점 (피크의 밸리)의 기저선으로부터의 높이
분리계수 크로마토그램에서 피크들 사이의 유지시간의 관계를 나타내는 것으로 분리계수 α는 다음 식으로 정의한다. 분리계수 α는 두 물질의 분배의 열역학적 차이의 지표로서 기본적으로는 두 물질의 분배평형계수의 비 또는 두 물질의 질량분포비의 비이지만 두 물질의 유지시간의 비로서 크로마토그램으로부터 구한다.
tR1 , tR2 : 분리도측정에 쓰는 2 개의 물질의 유지시간. 다만 tR1 < tR2
t0 : 이동상의 칼럼 통과시간 (k = 0인 물질을 주입한 때부터 그 물질의 피크정점까지의 시간)
분리도 크로마토그램에서 피크들 사이의 유지시간과 각각의 피크폭과의 관계를 나타내는 것으로 분리도 RS 로서 다음 식으로 정의한다.
tR1, tR2 : 분리도 측정에 쓰는 두 개의 물질의 유지시간. 다만 tR1 < tR2
W0.5h1, W0.5h2 : 각각의 피크높이의 1/2 위치에서의 피크폭
다만 tR1 , tR2, W0.5h1 및 W0.5h2 는 같은 단위를 쓴다.
이론단수 칼럼에서 물질의 밴드가 넓어지는 정도를 나타내는 것으로 보통 이론단수 N으로서 다음 식으로 정의한다.
tR : 물질의 유지시간
W0.5h : 피크높이의 1/2 위치에서의 피크폭.
다만 tR 및 W0.5h는 같은 단위를 쓴다.
주 의 표준피검물질, 내부표준물질 및 시험에 쓰는 시약․시액은 측정을 방해하는 물질을 함유하지 않은 것을 쓴다.
5. 납시험법
납시험법은 검체중에 들어있는 납(Pb)의 양의 한도를 시험하는 방법이다. 그 한도는 납으로서 중량백만분율(ppm)로 나타낸다.
조 작 법 따로 규정이 없는 한 원료각조에서 규정한 양의 검액을 취하여 납시험법용구연산암모늄시액 2㎖ 및 메칠레드시액 2방울을 넣고 액이 황색을 나타낼 때까지 강암모니아수를 넣는다. 여기에 납시험법용아황산나트륨시액 10㎖ 및 시안화칼륨시액 10㎖를 넣어 잘 흔들어 섞어 수욕상에서 10~15분간 가열한다. 식힌 다음 강암모니아수 1.5㎖를 넣어 분액깔때기로 옮기고 디티존․벤젠시액 10㎖를 정확하게 넣고 1분간 강하게 흔들어 섞은 다음 물층을 버린다. 여기에 묽은시안화칼륨시액 40㎖를 넣어 30초간 강하게 흔들어 섞어 방치한 다음 벤젠층을 따로 취 하여 벤젠을 대조로 하여 층장 10㎜, 파장 520㎚에서 흡광도를 측정한다. 따로 디티존용납표준액을 같은 방법으로 처리하여 얻은 검량선에 따라 납(Pb)의 양을 구한다.
주 의 : 1) 시험 및 검액조제에 쓰이는 시약 및 시액은 공시험에서 정색치 않거나 또는 거의 정색하지 않는 것을 쓴다.
2) 검체가 철염인 경우에는 납시험법용구연산암모늄시액은 10㎖, 납시험법용아황산나트륨시액은 20㎖ 및 시안화칼륨시액은 20㎖로 한다.
6. 레이크시험법
레이크시험법은 레이크색소의 확인시험(색소 자체의 확인 및 색소 자체에 결합 또는 흡착하고 있는 금속염 또는 금속의 확인), 순도시험 및 색소의 정량법으로 되어 있다.
확인시험 1) 색소의 확인 레이크에 사용 된 색소자체의 확인 검체 0.1 g을 달아 묽은수산화나트륨시액 10 mL를 넣어 섞고 필요하면 가온하여 색소를 용출시킨다. 불투명할 경우 원심분리하고, 용액 또는 상징액 5 mL를 취하여 희석액을 넣어 50 mL로 하여 검액으로 한다. 희석액에는 색소 확인시험의 흡광도측정법에서 사용한 시액 또는 용매를 사용한다.
가) 검액을 가지고 자외가시부흡광도측정법에 따라 흡수극대 파장을 측정할 때 각각의 색소의 흡수극대 파장이 같은 것을 확인한다.
나) 검액을 가지고 박층크로마토그래프법 제 1 법 또는 제 2 법에 따라 시험할 때 검액의 주반점은 각 색소의 확인시험에 기재된 색을 나타내며, 확인시험에서 표준액의 주반점과 같은 Rf 값을 나타내거나 확인시험에 기재된 Rs 값을 나타낸다.
2) 결합 또는 흡착하고 있는 금속 및 금속염의 확인
가) 알루미늄의 확인 검체 0.5 g을 달아 500 ℃로 강열 회화하여 얻은 잔류물에 묽은염산 20 mL를 넣고 가온한다. 이 액을 원심분리하여 얻은 상징액에 염화암모늄시액 및 암모니아시액을 넣을 때 흰색의 겔 침전이 생기고, 과량의 암모니아 시액을 추가해도 침전이 녹지 않는다.
나) 바륨의 확인 검체 0.5 g을 달아 500 ℃로 강열 회화하여 얻은 잔류물에 무수탄산나트륨 2 g 및 탄산칼륨 2 g을 넣고 잘 섞어서 가열하고 융해한다. 상온이 될 때 까지 식힌 다음 온수 10 mL를 넣어 섞고 여과한다. 여과지상의 잔류물을 온수로 씻고, 이 잔류물에 아세트산 2 mL를 넣어 녹이고 묽은 황산을 넣을 때 흰색의 침전이 생기고 묽은 질산을 추가해도 침전이 녹지 않는다.
다) 지르코늄의 확인 ① 검체 0.5 g을 달아 500 ℃로 강열 회화하여 얻은 잔류물에 황산 2 mL 및 황산암모늄 2 g을 넣고 가열하여 녹인다. 상온이 될 때까지 식힌 다음 가열된 묽은염산 5 mL를 넣어 검액으로 한다. 검액 2 mL에 β-니트로소-α-나프톨의 에탄올용액(1 → 50) 3 방울을 넣고 가온할 때 액이 등적색∼등갈색을 나타낸다.
② ①의 검액 2 mL에 물 5 mL 및 만델산용액(4 → 25)2 mL를 넣어 흔들고 섞을 때 흰색의 침전이 생긴다.
순도시험 1) 염산 및 암모니아 불용물시험법 검체 약 2 g을 정밀하게 달아 물 20 mL를 넣어 녹인 다음 염산 20 mL를 넣어 잘 섞고 끓여 식힌 물 300 mL를 넣어 잘 섞는다. 시계접시로 덮고 수욕에서 30 분간 가열한 다음 이것을 실온이 될 때까지 방치하여 식히고 원심분리한다. 이것의 상징액을 미리 질량을 알고 있는 도가니 형태의 유리여과기(1G4)로 여과하고, 물 약 30 mL로 불용물을 도가니 형태의 유리여과기에 옮기고, 물 5 mL씩으로 2 회 씻어서, 희석한 암모니아수(28)(1 → 25)로 씻은 액이 거의 무색으로 될 때까지 씻은 다음, 묽은염산(1 → 30) 10 mL로 씻고, 씻은 액이 변하지 않을 때까지 질산은시액으로 충분히 씻고, 도가니 형태의 유리여과기와 함께 105 ℃에서 3 시간 건조하고, 데시케이터(실리카겔)에서 실온이 될 때까지 식힌 다음 정밀하게 단다.
2) 수용성염화물 및 수용성황산염
가) 수용성염화물시험법 검체 약 2 g을 정밀하게 달아 물 200 mL를 넣고 약 30 분간 잘 흔들어 섞은 다음 건조여과지로 여과한다. 여과액이 착색 될 때까지 이것에 활성탄 2 g을 넣고 마개를 하여 잘 흔들고 섞은 다음 때때로 흔들고 섞으면서 1 시간 방치한 다음 여과한다. 여액이 무색으로 되지 않을 경우에는 무색으로 될 때까지 활성탄을 넣어 같은 조작을 반복한다. 이 여액을 검액으로 한다. 검액 50 mL를 250 mL 플라스크에 정확하게 취하여 묽은질산(38 → 100) 2 mL를 넣고 0.1 mol/L 질산은액 10 mL(염화물의 양이 많을 때에는 양을 늘인다)를 넣은 다음 니트로벤젠 약 5 mL를 넣는다. 그 다음 염화은이 석출될 때까지 흔들어 섞고 황산암모늄철(III)시액 1 mL를 넣고, 남은 질산은을 0.1 mol/L 티오시안산암모늄액으로 적정한다. 따로 같은 방법으로 공시험하고 다음 식에 따라 염화물의 양을 구한다.
A: 0.1 mol/L 티오시안산암모늄액의 소비량(mL)
A0 : 공시험에 있어서 0.1 mol/L 티오시안산암모늄액의 소비량(mL)
나) 수용성황산염시험법 검체 약 2 g을 정밀하게 달아 물 약 200 mL를 넣어 녹이고 활성탄 10 g을 넣고 흔들어 섞은 다음, 3분간 가만히 끓이고, 방치하여 식힌 다음 묽은질산(1 → 2) 1 mL를 넣어 잘 흔들고 섞은 다음, 흡인 여과하고, 소량의 물로 씻어낸 뒤, 여과액에 물을 넣어 250 mL로 한다. 이 액을 미리 양이온 교환수지(H 형)에 5 mL 이상 20 mL 이하로 충전하고, 내경 8 mm 이상 15 mm 이하의 칼럼관에 1분간 2 mL 이상 5 mL 이하의 유량으로 통과시키고, 처음의 유출액 30 mL를 버린 다음, 유출액을 검액으로 한다. 검액 50 mL를 정밀하게 달아 묽은염산 1 방울 또는 2 방울을 넣고 끓이면서 0.01 mol/L 염화바륨액 10 mL를 넣고 수분간 끓인 다음 방치하여 식히고 여기에 암모니아ㆍ염화암모늄완충액(pH 10.7) 5 mL, 암모니아ㆍ염화암모늄완충액(pH 10.7) 5 mL, 에틸렌디아민테트라아세트산디나트륨마그네슘사수화물 용액(4.3 → 100) 5 mL 및 에리오크롬블랙T시액 4 방울 또는 5 방울을 넣은 뒤, 0.01 mol/L 에틸렌디아민테트라아세트산이수소디나트륨시액으로 용액의 색이 청자색이 될 때까지 적정한다. 따로 같은 방법으로 공시험하고, 다음 식에 따라 황산염의 양을 구한다.
b:공시험에 있어서 0.01 mol/L 에틸렌디아민테트라아세트산이수소디나트륨시액의 소비량(mL)
c:0.01 mol/L 에틸렌디아민테트라아세트산이수소디나트륨 액의 소비량(mL)
k : Na2SO4 =1.4204, CaSO4=1.3614, K2SO4=1.7426, (NH4)2SO4= 1.3214
3) 수용성바륨시험법 검체 1.0 g을 달아 물 20 mL를 넣고 흔들어 섞어, 30 분간 방치한 다음 여과한다. 여과액 10 mL에 아세트산ㆍ아세트산나트륨시액 0.5 mL 및 크롬산칼륨시액 1 mL를 넣고 섞어, 10 분간 방치할 때 혼탁 또는 침전이 생긴다.
4) 수용성지르코늄시험법 검체 1.0 g을 달아 물 20 mL를 넣고 흔들어 섞어 30 분간 방치한 다음 여과한다. 여과액 10 mL에 묽은염산 1 mL와 만델산 용액(3 → 20) 5 mL를 가하고 수욕에서 가온할 때, 혼탁 또는 침전이 생긴다.
5) 비소시험법 각각의 색소의 비소시험법에 따라 시험한다.
6) 아연시험법 이 약을 가지고 원자흡광광도법의 전처리법 1)에 따라 조작하고 검액조제법 1)에 따라 조작한 것을 검액으로 한다. 따로 아연 표준원액(원자흡광광도법용) 5 mL를 취하여 묽은염산(1 → 4)을 넣어 10 mL로 하고 이 액 1 mL를 취하여 원자흡광광도법의 전처리법 1)에 따라 조작하고 검액조제법 1)에 따라 조작한 것을 비교액으로 하여 원자흡광광도법에 따라 시험할 때 500 ppm 이하이다.
7) 철시험법 이 약을 가지고 원자흡광광도법의 전처리법 1)에 따라 조작하고 검액조제법 1)에 따라 조작한 것을 검액으로 한다. 따로 철 표준원액(원자흡광광도법용) 1 mL를 취하여 묽은염산(1 → 4)을 넣어 10 mL로 하고 이 액 5 mL를 취하여 원자흡광광도법의 전처리법 1)에 따라 조작하고 검액조제법 1)에 따라 조작한 것을 비교액으로 하여 원자흡광광도법에 따라 시험할 때 500 ppm 이하이다.
8) 중금속시험법 이 약 2.5 g을 사기도가니에 넣고 황산 소량을 넣어 습윤하고 천천히 가열하여 거의 회화시킨 다음 실온까지 식히고 황산 1 mL를 넣어 천천히 가열하여 황산의 증기가 거의 나지 않게 한 다음 잔류물이 거의 백색이 될 때까지 450 ∼ 500 ℃로 강열한다. 여기에 염산 5 mL 및 질산 1 mL를 넣어 굳은 것을 잘 분쇄하여 수욕에서 증발 건고한 다음 여기에 염산 5 mL를 넣어 다시 굳은 것을 잘 분쇄하여 수욕에서 증발 건고한다. 잔류물에 10 % 염산 10 mL를 넣어 가열하여 녹이고 실온까지 식힌 다음 정량분석용여지를 써서 여과한다. 여지위의 잔류물을 10 % 염산 30 mL로 씻고 씻은 액을 위의 여액에 합하고 수욕에서 증발건고하고 10 % 염산 10 mL를 넣어 가열하고 녹이고 실온까지 식힌 다음 여과한다. 사기도가니 및 정량분석용여지를 소량의 물로 씻은 다음 씻은 액을 위의 여액에 합하여 10 % 아세트산암모늄시액으로 pH는 약 4로 조절한 다음 물을 넣어 100 mL로 하여 검액으로 한다. 따로 같은 조작을 하여 공시험액을 만든다. 검액 40 mL를 네슬러관에 취하여 물을 넣어 50 mL로 하여 검액으로 한다. 따로 공시험액 40 mL 및 납표준액 2 mL를 취하여 물을 넣어 50 mL로 하고 비교액으로 한다. 검액 및 비교액에 황화나트륨 시액 2 방울씩을 넣어 잘 흔들어 섞고 직사광선을 피하여 5 분간 방치한 다음 백색의 배경을 써서 네슬러관의 위 및 옆에서 관찰할 때 검액의 색은 비교액의 색보다 진하여서는 안된다 (20 ppm 이하).
정 량 법 이 약 약 20 mg ∼ 100 mg을 정밀하게 달아 묽은수산화나트륨시액 2.5 mL를 넣고, 필요하면 가온하거나 교반한 다음 원심분리를 하여 상층액을 취한다. 이 조작을 4회 반복하여 얻어진 상층액을 합한다. 이 액을 묽은염산(1 → 20)으로 중화시키고 각 순색소의 정량법에 사용한 희석액을 넣어 정확하게 200 mL로 한다. 필요하면 여과하고, 이 액을 검액으로 하여 각 순색소의 정량법에 따라 시험을 한다. 다만, 검액의 농도가 적절하지 않은 경우 검체 채취량을 조절할 수 있다.
7. 물가용물시험법
물가용물시험법은 검체중의 물에 녹는 물질의 양을 측정하는 방법이다.
조작법 따로 규정이 없는 한 검체 약 5g을 정밀하게 달아 물 약 70㎖를 넣어 5분간 끓인다. 식힌 다음 물을 넣어 100㎖로 하고 잘 저어 섞은 다음 여과한다. 처음의 여액 약 10㎖를 버리고 다음의 여액 40㎖를 정확하게 취하여 수욕상에서 증발건고하고 105∼110℃에서 1시간 건조한 다음 그 무게를 정밀하게 단다.
8. 미생물한도시험법
미생물한도시험법은 생균수시험 및 특정미생물시험을 포함한다. 원료 또는 제제에서 임의로 선택한 다른 수 개소 (또는 부분)에서 채취한 것을 잘 섞어 검체로 하여 시험한다. 검체를 액체배지로 희석할 때는 신속하게 시험한다. 또한 이 시험을 할 때에는 생물학적 위해가 일어나지 않도록 충분히 조심한다.
비무균제품의 미생물학적시험 : 생균수시험
1) 서문 이 시험은 호기조건에서 증식할 수 있는 중온성 (中溫性)의 세균 및 진균을 정량적으로 측정하는 방법이다. 이 시험은 원료 또는 제제가 규정된 미생물학적 품질규격에 적합한지 여부를 판정하는 것을 주 목적으로 한다. 채취검체수를 포함하여 지시된 시험방법에 따라 시험하여 결과를 판정한다. 생균을 유효성분으로 함유하는 제품에는 이 시험을 적용하지 않는다. 약전시험법과 동등성이 인정되는 경우에 자동화법을 포함한 다른 미생물학적방법을 적용할 수 있다.
2) 기본조작 생균수 측정은 검체가 외부로부터의 미생물 오염을 방지할 수 있도록 설계된 조건에서 시험한다. 오염을 방지하기 위한 예방조치는 시험에서 검출하고자하는 어떤 미생물에 대해서도 영향을 주어서는 안 된다. 검체가 항균활성을 가지고 있을 때는 항균활성을 가능한 한 제거 또는 중화한다. 이를 위해 불활성화제를 쓸 때는 그 불활성화제가 유효성이 있으며, 미생물에 대한 독성이 없음을 확인한다. 검체의 조제에 계면활성제를 쓸 때는 미생물에 대한 독성이 없으며 또한 사용하는 불활성화제와 상호작용이 없음을 확인한다.
3) 생균수측정법 보통 멤브레인필터법 또는 한천평판법을 쓴다. 최확수 (Most Probable Number ; MPN)법은 대체로 정밀도가 낮은 균수 측정법이기는 하나 오염균수가 아주 적은 검체에 대해서는 최적의 방법이 될 수도 있다. 측정법의 선택은 검체의 특성과 규정된 미생물한도값 등에 근거하며, 선택한 측정법은 규격에 적합한지 여부를 판단하기에 충분한 양의 검체를 시험할 수 있어야 하고 적합성이 확인되어야 한다.
4) 배지성능, 측정법의 적합성 및 음성대조
가) 일반요건 검체 존재 하의 미생물 검출능력을 확인한다. 그리고 시험결과에 영향을 주는 시험법의 변경이나 검체의 처방변경이 있는 경우에는 다시 적합성을 확인한다.
나) 시험균의 조제 시험균은 표준화된 안정한 현탁액을 사용하거나 다음과 같은 방법으로 조제한다. 시험에 쓰는 미생물은 최초의 마스터시드로트 (master seed lot)로부터 계대수 5 회를 넘지 않도록 시드로트 배양관리수법 (seed lot system)으로 관리한다. 세균 및 진균의 각 시험균에 대하여 표 I-1에 기재한 조건으로 각각 따로 배양한다.
표 I-1 시험균의 조제와 사용법
미생물 | 시험균의 조제 | 배지성능 | 제품존재 하에서의 생균수 측정법의 적합성 | ||
총호기성 미생물수 | 총진균수 | 총호기성 미생물수 | 총진균수 | ||
Staphylococus aureus 예를 들면, ATCC 6538, NCIMB 9518, CIP4.83, NBRC 13276 또는 KCTC 3881 | 대두카제인소화한천배지 또는 대두카제인소화액체배지 30 ∼ 35 ℃ 18 ∼ 24 시간 | 대두카제인소화한천배지 그리고 대두카제인소화액체배지 ≦ 100 CFU 30 ∼ 35 ℃ ≦ 3 일간 | | 대두카제인소화한천배지 / MPN대두카제인소화액체배지 ≦ 100 CFU 30 ∼ 35 ℃ ≦ 3 일간 | |
Pseudomonas aeruginosa 예를 들면, ATCC 9027, NCIMB 8626, CIP 82.118, NBRC 13275 또는 KCTC 2513 | 대두카제인소화한천배지 또는 대두카제인소화액체배지 30 ∼ 35 ℃ 18 ∼ 24 시간 | 대두카제인소화한천배지 그리고 대두카제인소화액체배지 ≦ 100 CFU 30 ∼ 35 ℃ ≦ 3 일간 | | 대두카제인소화한천배지 / MPN대두카제인소화액체배지 ≦ 100 CFU 30 ∼ 35 ℃ ≦ 3 일간 | |
Bacillus subsilis 예를 들면, ATCC 6633, NCIMB 8054, CIP 52.62, NBRC 3134 또는 KCTC 1021 | 대두카제인소화한천배지 또는 대두카제인소화액체배지 30 ∼ 35 ℃ 18 ∼ 24 시간 | 대두카제인소화한천배지 또는 대두카제인소화액체배지 ≦ 100 CFU 30 ∼ 35 ℃ ≦ 3 일간 | | 대두카제인소화한천배지 / MPN대두카제인소화액체배지 ≦ 100 CFU 30 ∼ 35 ℃ ≦ 3 일간 | |
Candida albicans 예를 들면, ATCC 10231, NCPF 3179, IP 48.72, NBRC 1594 또는 KCTC 7965 | 사부로포도당한천배지 또는 사부로포도당액체배지 20 ∼ 25 ℃ 2 ∼ 3 일간 | 대두카제인소화한천배지 ≦ 100 CFU 30 ∼ 35 ℃ ≦ 5일간 | 사부로포도당한천배지 ≦ 100 CFU 20 ∼ 25 ℃ ≦ 5일간 | 대두카제인소화한천배지 ≦ 100 CFU 30 ∼ 35 ℃ ≦ 5일간 MPN : 적용하지 않는다. | 사부로포도당한천배지 ≦ 100 CFU 20 ∼ 25 ℃ ≦ 5일간 |
Aspergillus brasiliensis 예를 들면, ATCC 16404, IMI 149007, IP 1431.83, NBRC 9455, KCTC 6317 또는 KCTC 6196 | 사부로포도당한천배지 또는 감자덱스트로오스한천배지 20 ∼ 25 ℃ 5 ∼ 7 일간 또는 양호한 포자형성이 인정될 때 까지 | 대두카제인소화한천배지 ≦ 100 CFU 30 ∼ 35 ℃ ≦ 5 일간 | 사부로포도당한천배지 ≦ 100 CFU 20 ∼ 25 ℃ ≦ 5일간 | 대두카제인소화한천배지 ≦ 100 CFU 30 ∼ 35 ℃ ≦ 5 일간 MPN : 적용하지 않는다. | 사부로포도당한천배지 ≦ 100 CFU 20 ∼ 25 ℃ ≦ 5 일간 |
시험균 현탁액의 조제는 pH 7.0 펩톤염화나트륨완충액 또는 pH 7.2 인산완충액을 쓴다. Asperigillus brasiliensis의 포자를 현탁할 때는 완충액에 폴리소르베이트 80을 0.05 % 넣어도 된다. 현탁액은 2 시간 이내에 쓰며 2 ∼ 8 ℃로 보존하는 경우에는 24 시간 이내에 쓴다. Asperigillus brasiliensis 또는 Bacillussubtilis의 영양형세포의 신선한 현탁액을 조제하여 희석하는 것을 대신 포자현탁액 또는 아포현탁액을 조제하여 접종균액으로 쓸 수 있다. 각 현탁액은 보증된 기간 내에서는 2 ∼ 8 ℃로 보존할 수 있다.
다) 음성대조 시험조건을 확인하기 위해 검액 대신 사용한 희석액을 써서 음성대조시험을 한다. 미생물이 증식해서는 안 된다. 음성대조는 5)항에 따른 검체시험 시에도 측정한다. 시험에 실패한 음성대조는 고찰한다.
라) 배지성능 시판배지는 배치마다 시험한다. 건조분말배지 또는 기술한 각 성분을 써서 조제한 배지는 조제한 배치마다 시험한다. 표 I-1에 기재한 미생물의 소량 (100 CFU 이하)을 대두카제인소화액체배지의 일부, 대두카제인소화한천배지 및 사부로포도당한천배지의 평판에 접종한다. 균주마다 별개로 액체배지 또는 평판을 써서 표 I-1에 기재한 조건으로 각각 배양한다. 한천배지에서는 접종균의 출현집락수가 표준화된 균액의 측정값의 1/2 ∼ 2 배 이내 이어야 한다. 신선한 배양균을 써서 시험하는 경우에는 유효성이 확인된 배지 배치에서 이전에 얻은 증식과 동등한 증식이 인정되어야 한다. 액체배지에서도 유효성이 확인된 배지 배치로 미리 시험하여 얻은 증식과 동등한 증식이 인정되어야 한다.
마) 검체 존재 하의 측정법의 적합성
① 검액의 조제 검액의 조제법은 검체의 물리학적 특성에 의존한다. 아래에 기재한 어느 방법도 만족할 수 없을 때에는 따로 적절한 다른 방법을 확립한다.
ⅰ) 수용성제제 검체를 pH 7.0 펩톤염화나트륨완충액, pH 7.2 인산완충액 또는 대두카제인소화액체배지로 녹이거나 희석한다 (보통 10 배 희석액을 조제한다). 필요하면 pH 6 ∼ 8로 조정한다. 희석이 더 필요할 때에는 같은 희석액으로 조제한다.
ⅱ) 물에 녹지 않는 비지질제제 검체를 pH 7.0 펩톤염화나트륨완충액, pH 7.2 인산완충액 또는 대두카제인소화액체배지에 현탁한다 (보통 10 배 희석액을 조제한다). 분산하기 쉽게 하기 위해 예를 들면 폴리소르베이트 80 (농도 : 1 g/L)과 같은 계면활성제를 넣을 수 있다. 필요하면 pH 6 ∼ 8로 조정한다. 희석이 더 필요할 때에는 같은 희석액으로 조제한다.
ⅲ) 지질제제 검체를 여과멸균한 이소프로필미리스테이트에 녹이거나 필요하면 40 ℃ 이하 (예외적인 경우에는 45 ℃ 이하)에서 가온한 최소필요량의 멸균된 폴리소르베이트 80 또는 다른 저해성이 없는 계면활성제를 써서 혼합한다. 필요하면 수욕에서 그 온도를 유지하면서 주의깊게 섞는다. 선정한 희석액을 미리 가온하여 넣어 검체의 10 배 희석액을 조제한다. 유화에 필요한 가장 짧은 시간 동안 온도를 유지하면서 주의하여 섞는다. 적절한 농도의 멸균한 폴리소르베이트 80 또는 다른 저해성이 없는 계면활성제를 함유하는 같은 희석액으로 10 배 단계 희석계열을 조제해도 된다.
ⅳ) 에어로솔형의 액체 또는 고체 검체를 무균적으로 멤브레인필터장치에 넣거나 검체 채취를 위해 멸균용기로 옮긴다. 각 검체용기에서 전량을 쓰거나 정량분무한 일정량을 쓴다.
ⅴ) 경피흡수패취 경피흡수패취의 보호피복 (박리라이너)을 제거하고 점착면을 위로 향하게 하여 멸균유리 또는 멸균플라스틱트레이 (tray) 위에 놓는다. 패취끼리 부착하는 것을 막기 위해 멸균한 다공성물질 (예를 들면 멸균거즈)로 점착면을 덮는다. 폴리소르베이트 80 및/또는 레시틴 등의 불활성화제를 함유하는 선정한 희석액 적당량에 패취를 넣고 적어도 30 분간 세게 흔들어 섞는다.
② 접종 및 희석 100 CFU 이하의 접종균을 얻는데 충분한 양의 시험균 현탁액을 ①항에 따라 조제한 검액 및 대조액 (검체 불포함)에 넣는다. 접종하는 시험균 현탁액의 양은 검액량의 1 %를 초과하지 않도록 한다. 제품에서 허용가능한 미생물 회수결과를 얻기 위해 가장 낮은 희석배율의 검액을 가지고 시험한다. 항균활성 또는 낮은 용해도 때문에 가장 낮은 희석배율의 검액으로 시험할 수 없는 경우에는 다시 적절한 시험방법을 확립한다. 검체로 인한 증식저지를 피할 수 없는 경우에는 중화, 희석 또는 여과한 다음에 시험균 현탁액을 넣어도 된다.
③ 항균활성의 중화ㆍ제거 ② 및 ④항에 기재한 방법에 따라 시험하여 검액에서 회수한 균수와 대조액에서 회수한 균수를 비교한다. 증식이 저해되는 경우 (검액에서 회수한 균수가 대조액에서 회수한 균수의 1/2 미만인 경우)에는 결과의 유효성을 확보하기 위해 생균수 측정법을 변경한다. 방법의 변경은 예를 들어 (1) 희석액 또는 배지의 증량, (2) 특이적 또는 일반적인 중화제를 희석액에 첨가, (3) 막여과 또는 (4) 위의 측정법의 조합 등이다.
중화제 항균제의 활성을 중화하기 위해 중화제를 쓸 수 있다 (표 I-2). 중화제는 선정한 희석액 또는 배지에 멸균 전에 미리 첨가할 수 있다. 중화제를 쓴 경우에는 그 유효성과 미생물에 대한 독성이 없음을 증명하기 위해 검체를 함유하지 않고 중화제만을 넣어 공시험하여 확인한다.
표 I-2 저해물질에 대한 일반적인 중화제/중화법
저해물질 | 중화제/중화법 |
글루타르알데히드, 수은제 | 아황산수소나트륨 |
페놀류, 알코올류, 알데히드류, 소르빈산염 | 희석 |
알데히드류 | 글리신 |
4급 암모늄 화합물, 파라옥시벤조산류, 비스-비구아니드류 | 레시틴 |
4급 암모늄 화합물, 파라옥시벤조산류, 요오드 | 폴리소르베이트 |
수은제 | 티오글리콜산염 |
수은제, 할로겐류, 알데히드류 | 티오황산염 |
에틸렌디아민테트라아세트산염 (EDTA) | 마그네슘 또는 칼슘이온 |
적절한 중화법을 확립할 수 없는 경우에는 그 검체가 가지는 항균활성 때문에 접종균을 분리할 수 없는 것으로 간주한다. 따라서 그 검체가 접종균과 같은 종의 균이나 근연종에 오염되었을 가능성은 낮은 것으로 생각한다. 그러나 그 검체가 이들 일부 미생물만을 저해할 뿐이고, 시험균주 이외의 균주는 저해하지 않을 가능성도 있으므로 미생물의 증식과 그 허용기준에 적합한 가장 낮은 농도로 시험한다.
④ 검체에서의 미생물 회수 표 I-1 에 기재된 미생물마다 따로 시험한다. 첨가한 미생물만을 대상으로 측정한다.
i) 멤브레인필터법 공경 0.45 μm 이하의 멤브레인필터를 쓴다. 필터의 재질은 검체의 성분에 의하여 세균포집능력이 영향을 받지 않도록 주의하여 선택한다. 표 I-1의 각 미생물마다 1 개의 멤브레인필터를 쓴다. ① ∼ ③항에 따라 조제한 검체의 적당량 (가능하면 검체의 1 g 해당량 또는 다수의 집략형성이 예측되는 경우에는 그 이하)을 멤브레인필터에 넣어 바로 여과하고 적당량의 희석액으로 멤프레인필터를 씻는다. 멤브레인필터를 총호기성미생물수 (total aerobic microbial count ; TAMC) 측정용으로는 대두카제인소화한천배지의 표면으로, 총진균수 (total combined yeasts/mould count : TYMC) 측정용으로는 사부로포도당한천배지의 표면으로 옮긴다. 표 I-1 에 기재한 조건으로 이들 평판을 배양한 다음 집락수를 측정한다.
ii) 한천평판법 한천평판법은 각 배지에 대하여 적어도 2 개의 평판을 써서 시험하며 결과는 각 평판의 측정균수의 평균값을 사용한다.
가. 한천평판혼합법 지름 9 cm의 페트리접시를 쓸 때는 페트리접시에 ① ∼ ③항에 따라 조제한 검체 1 mL 및 미리 45 ℃ 이하로 보온한 15 ∼ 20 mL의 대두카제인소화한천배지 또는 사브로포도당한천배지를 넣는다. 보다 큰 페트리접시를 쓸 때에는 크기에 맞게 한천배지량을 증가한다. 표 I-1에 제시한 미생물마다 적어도 2 개의 페트리접시를 쓴다. 표 I-1에 기재한 조건으로 평판배지를 배양한다. 배지마다 균주의 산술평균을 가지고 집락수를 계산한다.
나. 한천평판도말법 지름 9 cm의 페트리접시를 쓸 때는 15 ∼ 20 mL의 대두카제인소화한천배지 또는 사부로포도당한천배지를 약 45 ℃일 때 넣어 굳힌 다음 층류식 캐비넷이나 항온기 중에서 평판배지를 건조한다. 보다 큰 페트리접시를 쓸 때에는 크기에 맞게 한천배지량을 증가한다. 표 I-1에 기재한 미생물마다 적어도 2 개의 페트리접시를 쓴다. ① ∼ ③항에 따라 조제한 검체 0.1 mL 이상을 정확하게 취하여 배지표면전체에 편다. ii) 가.에 기재한 것과 같이 배양하여 측정한다.
iii) 최확수법 최확수법의 정밀도 및 정확도는 멤브레인필터법 또는 한천평판법 보다 낮다. 특히 곰팡이를 측정할 때는 신뢰성이 낮다. 이러한 이유로 최확수법은 다른 방법의 이용이 불가능할 때의 총호기성미생물수의 측정에 이용한다. 이 법을 적용할 때에는 다음과 같이 한다. ① ∼ ③항에 따라 검체의 적어도 각각 3 개씩의 10 배 단계 희석계열을 조제한다. 각 희석단계로부터 각각 1 g 또는 1 mL 씩을 취하고 대두카제인소화액체배지가 9 ∼ 10 mL 들어있는 3 개의 시험관에 각각 접종한다. 필요하면 폴리소르베이트 80과 같은 계면활성제 또는 항균제의 불활성화제를 배지에 첨가할 수 있다. 따라서 3 단계의 희석계열을 조제한 경우에는 9 개의 시험관에 접종하는 것이 된다. 모든 시험관을 30 ∼ 35 ℃에서 3 일을 넘지 않는 기간 동안 배양한다. 검체의 성질로 인해 결과의 판정이 곤란하거나 불확실한 경우에는 같은 배지 또는 대두카제인소화한천배지에 이식한 다음 같은 온도에서 1 ∼ 2 일간 배양하고 이 결과를 쓴다. 표 I-3 으로부터 검체 1 g 또는 1 mL 당 미생물의 최확수를 구한다.
표 I-3 미생물의 최확수
각 세트에서의 미생물 증식을 나타내는 시험관 수의 조합 | 제품 1 g 또는 1 mL 당의 최확수 | 95 % 신뢰한계 | ||
시험관 당 제품의 g 또는 mL 수 | ||||
0.1 | 0.01 | 0.001 | ||
0 | 0 | 0 | < 3 | 0 ∼ 9.4 |
0 | 0 | 1 | 3 | 0.1 ∼ 9.5 |
0 | 1 | 0 | 3 | 0.1 ∼ 10 |
0 | 1 | 1 | 6.1 | 1.2 ∼ 17 |
0 | 2 | 0 | 6.2 | 1.2 ∼ 17 |
0 | 3 | 0 | 9.4 | 3.5 ∼ 35 |
1 | 0 | 0 | 3.6 | 0.2 ∼ 17 |
1 | 0 | 1 | 7.2 | 1.2 ∼ 17 |
1 | 0 | 2 | 11 | 4 ∼ 35 |
1 | 1 | 0 | 7.4 | 1.3 ∼ 20 |
1 | 1 | 1 | 11 | 4 ∼ 35 |
1 | 2 | 0 | 11 | 4 ∼ 35 |
1 | 2 | 1 | 15 | 5 ∼ 38 |
1 | 3 | 0 | 16 | 5 ∼ 38 |
2 | 0 | 0 | 9.2 | 1.5 ∼ 35 |
2 | 0 | 1 | 14 | 4 ∼ 35 |
2 | 0 | 2 | 20 | 5 ∼ 38 |
2 | 1 | 0 | 15 | 4 ∼ 38 |
2 | 1 | 1 | 20 | 5 ∼ 38 |
2 | 1 | 2 | 27 | 9 ∼ 94 |
2 | 2 | 0 | 21 | 5 ∼ 40 |
2 | 2 | 1 | 28 | 9 ∼ 94 |
2 | 2 | 2 | 35 | 9 ∼ 94 |
2 | 3 | 0 | 29 | 9 ∼ 94 |
2 | 3 | 1 | 36 | 9 ∼ 94 |
3 | 0 | 0 | 23 | 5 ∼ 94 |
3 | 0 | 1 | 38 | 9 ∼ 104 |
3 | 0 | 2 | 64 | 16 ∼ 181 |
3 | 1 | 0 | 43 | 9 ∼ 181 |
3 | 1 | 1 | 75 | 17 ∼ 199 |
3 | 1 | 2 | 120 | 30 ∼ 360 |
3 | 1 | 3 | 160 | 30 ∼ 380 |
3 | 2 | 0 | 93 | 18 ∼ 360 |
3 | 2 | 1 | 150 | 30 ∼ 380 |
3 | 2 | 2 | 210 | 30 ∼ 400 |
3 | 2 | 3 | 290 | 90 ∼ 990 |
3 | 3 | 0 | 240 | 40 ∼ 990 |
3 | 3 | 1 | 460 | 90 ∼ 1980 |
3 | 3 | 2 | 1100 | 200 ∼ 4000 |
3 | 3 | 3 | > 1100 | |
바) 결과 및 판정 멤브레인필터법 또는 한천평판법의 적합성을 확인할 때 모든 시험균의 평균측정값이 ②항에서 정의한 대조액 (검체 불포함)의 측정값의 1/2 ∼ 2 배 이내이어야 한다. 최확수법의 적합성을 확인할 때에는 측정값은 대조에서 얻은 결과의 95 % 신뢰한계 범위 이내이어야 한다. 기술한 어떠한 방법에서도 시험균 하나 또는 그 이상의 균종에서 위의 기준을 충족시키지 못하는 경우에는 기준에 가장 근접한 방법과 시험조건으로 검체를 시험한다.
5) 검체의 시험
가) 시험량 따로 규정이 없는 한 위에 기술한 대로 주의하여 채취한 검체 10 g 또는 10 mL를 쓴다. 에어로솔형의 액체 또는 고체는 검체 10 용기를 취한다. 경피흡수패취는 검체 10 패취를 취한다. 투여단위 (예를 들면 정제, 캡슐제, 주사제) 당의 주성분량이 1 mg 이하이거나 또는 1 g 또는 1 mL (투여단위가 표시되지 않은 제제) 당의 활성성분량이 1 mg 미만인 경우는 시험량을 줄일 수 있다. 이 경우 피험검체의 채취량은 제품의 10 투여단위 혹은 10 g 또는 10 mL에 들어있는 양보다도 적지 않도록 한다. 주성분으로 사용되는 물질은 검체의 양에 제한이 있거나 로트 크기가 매우 작은 (예를 들면 1000 mL 또는 1000 g 미만) 경우에는 보다 적은 양이 규정되어 있거나 또는 정당한 이유가 없는 한 시험량은 로트의 1 %로 한다. 로트크기가 200 미만 (예를 들면 임상시험용 검체)인 검체에서는 시험량은 2 투여단위로, 또는 로트크기가 100 미만의 경우에는 1 투여단위로 줄일 수 있다. 원료 또는 제제의 용기로부터 무작위로 검체를 채취한다. 필요한 양의 검체를 얻기 위해 충분한 수의 용기의 내용물을 혼합한다.
나) 검체 시험
① 멤브레인필터법 필터를 배지에 넣을 수 있도록 설계된 여과장치를 쓴다. 4)에 따라 적합성이 확인된 방법으로 검체를 조제하고 적당량을 2 개의 멤브레인필터에 각각 넣고 바로 여과한다. 적합성이 확인된 방법에 따라 각 필터를 씻는다. 1 개의 멤브레인필터는 총호기성미생물수 측정을 위해 대두카제인소화한천배지의 표면에, 다른 한 개의 멤브레인필터는 총진균수 측정을 위해 사부로포도당한천배지의 표면에 놓는다. 대두카제인소화한천배지를 30 ∼ 35 ℃에서 3 ∼ 5일간, 사부로포도당배지를 20 ∼ 25 ℃에서 5 ∼ 7일간 배양한다. 검체 1 g 또는 1 mL 당의 집락수를 계산한다. 경피흡수패취를 시험할 때에는 4) 마)①항에 기재되어있는 조제액의 10 %량 씩을 2 개의 멸균멤브레인필터로 따로 여과한다. 1 개의 멤브레인필터는 총호기성미생물수 측정을 위해 대두카제인소화한천배지에 넣고 다른 한 개의 멤브레인필터는 총진균수 측정을 위해 사부로포도당한천배지에 넣는다.
② 한천평판법
ⅰ) 한천평판혼합법 4)항에 따라 적합성이 확인된 방법으로 검액을 조제한다. 각 배지에 대하여 희석단계마다 적어도 2 개의 페트리접시를 준비한다. 대두카제인소화한천배지는 30 ∼ 35 ℃에서 3 ∼ 5일간 배양하고 사부로포도당한천배지는 20 ∼ 25 ℃에서 5 ∼ 7 일간 배양한다. 집락수가 총호기성미생물수 측정에서는 250 미만, 총진균수 측정에서는 50 미만이면서 가장 많은 집락수를 나타내는 희석도의 한천배지를 선택하여 균수를 구한다. 배지마다 균수의 산술평균을 구하여 검체 1 g 또는 1 mL 당의 집락수를 계산한다.
ⅱ) 한천평판도말법 4)항에 따라 적합성이 확인된 방법으로 검액을 조제한다. 각 배지에 대하여 희석단계마다 적어도 2 개의 페트리접시를 준비한다. 배지 및 집락수의 계산은 한천평판혼합법에 기재된 대로 한다.
③ 최확수법 4)항에 따라 적합성이 확인된 방법으로 검액을 조제하여 희석한다. 모든 시험관을 30 ∼ 35 ℃에서 3 ∼ 5일간 배양한다. 필요하면 적합성이 확인된 방법으로 이식배양한다. 희석단계마다 미생물의 증식이 인정되는 시험관수를 기록한다. 표 I-3으로부터 검체 1 g 또는 1 mL 당 미생물의 최확수를 구한다.
다) 결과의 판정 대두카제인소화한천배지를 써서 측정된 집락수를 총호기성미생물수 (TAMC)로 한다. 이 배지 위에 진균의 집락이 검출되어도 TAMC로 계산한다. 사부로포도당한천배지를 써서 측정하는 집락수를 총진균수 (TYMC)로 한다. 이 배지위에 세균의 집락이 검출되어도 TYMC로서 계산한다. 세균의 증식 때문에 TYMC가 허용기준을 넘을 것으로 예측될 때에는 항생물질을 함유하는 사부로포도당한천배지를 써도 된다. 최확수법으로 측정하는 경우에는 계산값을 TAMC로 한다. 미생물학적 품질 허용기준이 규정되어 있을 때 아래와 같이 판정한다.
- 101 CFU : 최대허용 수 = 20
- 102 CFU : 최대허용 수 = 200
- 103 CFU : 최대허용 수 = 2000, 이하 동일
권장 용액 및 배지는 「특정미생물시험」에 기재되어 있다.
비무균제품의 미생물학적시험 : 특정미생물시험
1) 서문 이 시험은 규정된 조건에서 검출할 수 있는 특정미생물이 존재하지 않거나 그 존재가 한정적인지를 판정하는 방법이다. 이 시험은 원료나 제제가 이미 정해진 미생물학적품질규격에 적합한지의 여부를 판정하는 것을 주 목적으로 한다. 채취검체수를 포함하여 지시된 방법에 따라 시험하여 결과를 판정한다. 약전시험법과의 동등성이 인정되는 경우에는 자동화법을 포함한 다른 미생물학적 방법을 적용할 수 있다.
2) 기본조작 검체의 조제는 「생균수시험」에 따른다. 검체가 항균활성이 있을 때에는 「생균수시험」에서와 같이 이 항균활성을 제거 또는 중화한다. 검체의 조제에 계면활성제를 쓸 때에는 「생균수시험」에서와 같이 미생물에 대한 독성이 없고 사용하는 불활성화제와 상호작용이 없는 것을 확인한다.
3) 배지의 성능, 시험법의 적합성 및 음성대조 검체 존재 하에서도 미생물을 검출할 능력이 있음을 확인한다. 시험결과에 영향을 주는 시험법의 변경이나 검체의 처방변경이 있는 경우에는 다시 적합성을 확인한다.
가) 시험균의 조제 시험균은 표준화된 안정한 현탁액을 쓰거나 다음과 같은 방법으로 조제한다. 시험에 쓰는 미생물은 최초의 마스터시드로트 (master seed lot)로부터의 계대수가 5 회를 초과하지 않게 시드 로트 배양관리수법 (seed lot system)으로 관리한다.
① 호기성미생물 각 세균시험용 균주를 대두카제인소화액체배지 또는 대두카제인소화한천배지에서 각각 30 ∼ 35 ℃에서 18 ∼ 24 시간 배양한다. 칸디다알비칸스용의 시험균주는 사부로포도당한천배지 또는 사부로 포도당액체배지에서 각각 20 ∼ 25 ℃에서 2 ∼ 3 일간 배양한다.
Staphylococcus aureus (황색포도구균) : 예를 들면 ATCC 6538, NCIMB 9518, CIP 4.83, NBRC 13276 또는 KCTC 1927
Pseudomonas aeruginosa (녹농균) : 예를 들면 ATCC 9027, NCIMB 8626, CIP 82.118, NBRC 13275 또는 KCTC 2513
Escherichia coli (대장균) : 예를 들면 ATCC 8739, NCIMB 8545, CIP 53.126, NBRC 3972 또는 KCTC 2571
Salmonella enterica subsp. enterica serovar Typhimurium 또는 이와 동등한 것 (살모넬라) : 예를 들면 ATCC 14028
Salmonella enterica subsp. enterica serovar Abony (살모넬라) : 예를 들면 NBRC 100797, NCTC 6017 또는 CIP 80.39
Candida albicans (칸디다알비칸스) : 예를 들면 ATCC 10231, NCPF 3179, IP 48.72 또는 NBRC 1594, KCTC 7965
시험균 현탁액의 조제는 pH 7.0 펩톤염화나트륨완충액 또는 pH 7.2 인산완충액을 쓴다. 현탁액은 2 시간 이내에 쓰며, 2 ∼ 8 ℃에서 보존하는 경우에는 24 시간 이내에 쓴다.
② 클로스트리디아 예를 들면 ATCC 11437 (NBRC 14293, NCIMB 12343, CIP 100651) 또는 ATCC 17404 (NCTC 532 또는 CIP 79.3)와 같은 Clostridium sporogenes를 쓴다. 클로스트리디아 시험균주를 강화 클로스트리디아배지 중에 접종하고 30 ∼ 35 ℃에서 24 ∼ 48 시간 혐기적 조건에서 배양한다. Cl. Sporogenes의 영양형 세포의 신선현탁액을 조제하여 희석하는 대신에 아포현탁액을 접종균액으로 사용할 수 있다. 아포현탁액은 보증된 기간 내에서는 2 ∼ 8 ℃에서 보존할 수 있다.
나) 음성대조 시험조건을 확인하기 위해 검액 대신 사용한 희석액을 써서 음성대조시험을 한다. 미생물이 증식해서는 안된다. 음성대조는 5)항에 따른 검체시험 시에도 측정한다. 시험에 실패한 음성대조는 고찰한다.
다) 배지의 성능시험 시판배지는 배치마다 시험한다. 건조배지 또는 각 성분을 가지고 조제한 배지는 조제배치마다 시험한다. 표 II-1의 내용과 같이 관련 배지에 대하여 적절한 특성을 확인한다.
표 II-1 배지의 증식촉진, 증식억제 및 감별특성
배지 | 특성 | 시험균주 |
담즙산저항성그람음성균시험 | ||
모젤장내세균증균액체배지 | 증식촉진 | E. coli P. aeruginosa |
1.1.1.1. 증식억제 | S. aureus | |
바이올렛·레드·담즙산·포도당한천배지 | 증식촉진 및 감별 | E. coli P. aeruginosa |
대장균시험 | ||
맥콘키액체배지 | 증식촉진 | E. coli |
1.1.1.2. 증식억제 | S. aureus | |
맥콘키한천배지 | 증식촉진 및 감별 | E. coli |
살모넬라시험 | ||
라파포드바시리아디스살모넬라증균액체배지 | 증식촉진 | Salmonella enterica subsp. enterica serovar Typhimurium 또는 Salmonella enterica subsp. enterica serovar Abony |
1.1.1.3. 증식억제 | S. aureus | |
엑스엘디한천배지(XLD agar) | 증식촉진 및 감별 | Salmonella enterica subsp. enterica serovar Typhimurium 또는 Salmonella enterica subsp. enterica serovar Abony |
녹농균시험 | ||
세트리미드한천배지 | 증식촉진 | P. aeruginosa |
1.1.1.4. 증식억제 | E. coli | |
황색포도상구균시험 | ||
만니톨염화나트륨한천배지 | 증식촉진 및 감별 | S. aureus |
1.1.1.5. 증식억제 | E. coli | |
클로스트리디아시험 | ||
강화클로스트리디아배지 | 증식촉진 | Cl. sporogenes |
콜롬비아한천배지 | 증식촉진 | Cl. sporogenes |
칸디다알비칸스시험 | ||
사부로포도당액체배지 | 증식촉진 | C. albicans |
사부로포도당한천배지 | 증식촉진 및 감별 | C. albicans |
증식촉진특성시험, 액체배지 적당한 배지의 일부에 적절한 미생물을 소량 (100 CFU 이하) 접종한다. 규정된 온도에서 배양하고 배양시간은 시험법에서 규정되어 있는 배양기간 중 최단시간 이내로 한다. 유효성이 확인된 배지 배치에서 이전에 시험하여 얻은 증식과 동등한 증식을 확인한다.
증식촉진특성시험, 고체배지 각 평판배지에 적당한 미생물을 소량 (100 CFU 이하) 접종하고 한천평판도말법으로 시험한다. 규정된 온도에서 배양하고 배양시간은 시험법에 규정되어 있는 배양기간 중 최단시간 이내로 한다. 유효성이 확인된 배지 배치에서 이전에 시험하여 얻은 증식과 동등한 증식을 확인한다.
증식억제특성시험, 액체 또는 고체배지 적당한 배지에 적절한 미생물을 적어도 100 CFU 접종한다. 규정된 온도에서 배양하고 배양시간은 시험법에 규정되어 있는 배양기간 중 최장시간 이상으로 한다. 시험균의 증식이 확인되지 않는다.
감별특성시험 각 평판배지에 적당한 미생물을 소량 (100 CFU 이하) 접종하고 한천평판도말법으로 시험한다. 규정된 온도에서 배양하고 배양시간은 시험법에 규정되어 있는 배양기간의 범위 내로 한다. 집락의 형상과 감별반응은 유효성이 확인된 배지 배치에서 이전에 시험하여 얻은 것과 동등하다.
라) 시험법의 적합성 검체마다 4)항의 관련 항목에 기재되어 있는 대로 검액를 조제한다. 규정된 증균배지에 혼합할 때 각 시험균을 넣는다. 시험균은 개별적으로 접종한다. 접종한 시험액 중 100 CFU 이하에 해당하는 균수의 미생물을 쓴다. 4)항의 관련항목에 따라 시험한다. 다만 규정된 배양기간 중 최단시간으로 한다. 특정미생물은 4)항에 기재된 감별반응으로 검출되어야 한다. 검체의 항균활성이 인정되는 경우에는 시험방법의 변경이 필요하다 (「생균수시험」의 3) 마)③항 항균활성의 중화ㆍ제거 항 참조). 어떠한 특정검체에서 규정된 시험법으로 미생물에 대한 항균활성을 중화할 수 없는 경우에는 억제된 미생물이 그 검체 중에 존재하지 않는다고 간주해도 된다.
4) 검체의 시험
가) 담즙산저항성 그람음성균
① 검액 조제 및 전(前)배양 검체 1 g 이상을 달아 그 10 배 희석액을 「생균수시험」에 따라 조제하며, 이 때 희석액으로는 대두카제인소화액체배지를 써서 섞은 다음 균을 소생시키기에 충분하나 증균을 촉진시키지 않는 적절한 시간 (보통 2 시간이며 5 시간 이내) 동안 20 ∼ 25 ℃에서 배양한다.
②부정시험 따로 규정되어 있지 않으면 ①항에서 조제한 검체 1 g에 해당하는 검액을 모젤장내세균증균액체배지에 접종한다. 30 ∼ 35 ℃에서 24 ∼ 48 시간 배양한 다음 바이올렛·레드·담즙산·포도당한천배지에 이식하고 30 ∼ 35 ℃에서 18 ∼ 24 시간 배양한다. 집락의 증식이 없으면 검체는 이 시험에 적합하다.
③ 정량시험
i) 선택배양 ①항에 기재되어 있는 조제액 및/또는 그 희석액으로 각각 검체의 0.1 g, 0.01 g, 0.001 g (또는 0.1 mL, 001 mL, 0.001 mL) 해당량을 적당량의 모젤장내세균증균액체배지에 접종한다. 30 ∼ 35 ℃에서 24 ∼ 48 시간 배양 한 다음 바이오렛·레드·담즙산·포도당 한천배지에 각 배양액을 이식하고 30 ∼ 35 ℃에서 18 ∼ 24 시간 배양한다.
ii) 판정 집락의 증식이 인정된 경우에는 양성으로 판정한다. 양성결과로 나타난 검체의 최소량과 음성결과로 나타난 최대량을 기재하고 표 II-2로부터 세균의 추정값을 구한다.
표 II-2 결과의 판정
제품의 각 양에 대한 결과 | 제품 1 g 또는 1 mL당 세균의 추정수 | ||
0.1 g 또는 0.1 mL | 0.01 g 또는 0.01 mL | 0.001 g 또는 0.001 mL | |
+ | + | + | 103 보다 크다 |
+ | + | - | 103 보다 작고 102 보다 크다 |
+ | - | - | 102 보다 작고 10 보다 크다 |
- | - | - | 10 보다 작다 |
나) 대장균
① 검액의 조제 및 전배양 검체 1 g 이상을 취하여 「생균수시험」에 따라 조제한 10 배 희석액 10 mL 혹은 검체 1 g 또는 1 mL에 해당하는 양을 적당량 (3) 라) 시험법의 적합성에서 결정)의 대두카제인소화액체배지에 접종하고 섞은 다음 30 ∼ 35 ℃에서 18 ∼ 24 시간 배양한다.
② 선택배양 용기를 흔들며 대두카제인소화액체배지의 1 mL를 맥콘키액체배지 100 mL에 넣는다. 42 ∼ 44 ℃에서 24 ∼ 48 시간 배양한 다음 맥콘키한천배지에 이식하고 30 ∼ 35 ℃에서 18 ∼ 72 시간 배양한다.
③ 판정 집락의 증식이 인정될 때에는 양성으로 의심하고 동정시험으로 확인한다. 집락이 없거나 또는 동정시험에서 음성으로 판정될 때 검체는 이 시험에 적합하다.
다) 살모넬라
① 검액 조제 및 전배양 검체 10 g 또는 10 mL를 취하여 적당량 (3) 라) 시험법의 적합성에서 결정)의 대두카제인소화액체배지에 접종하고 섞은 다음 30 ∼ 35 ℃에서 18 ∼ 24 시간 배양한다.
② 선택배양 대두카제인소화액체배지 0.1 mL를 라파포트바시리아디스살모넬라 증균액체배지에 접종한다. 30 ∼ 35 ℃에서 18 ∼ 24 시간 배양한 다음 XLD 한천배지에 이식하고 30 ∼ 35 ℃에서 18 ∼ 48 시간 배양한다.
③ 판정 충분히 증식한 빨간색집락이 인정될 때에는 중심부에 흑점의 유무에 관계없이 양성으로 의심하고 동정시험으로 확인한다. 기재되어 있는 종류의 집락이 없거나 또는 동정시험에서 음성으로 판정될 때 검체는 이 시험에 적합하다.
라) 녹농균
① 검액조제 및 전배양 검체 1 g 이상을 취하고 「생균수시험」에 따라 조제한 10 배 희석액 10 mL 혹은 검체 1 g 또는 1 mL에 해당하는 양을 적당량 (3) 라) 시험법의 적합성에서 결정)의 대두카제인소화액체배지에 접종하여 섞은 다음 30 ∼ 35 ℃에서 18 ∼ 24 시간 배양한다. 경피흡수패취를 시험할 때는 「생균수시험」의 4) 마)①항에 기재한대로 조제하고 1 패취 해당량을 멸균멤브레인필터로 여과하고 이 멤브레인필터를 100 mL의 대두카제인소화액체배지 중에 넣는다.
② 선택배양 세트리미드한천배지에 이식하고 30 ∼ 35 ℃에서 18 ∼ 72 시간 배양한다.
③ 판정 집락의 증식이 인정될 때에는 양성으로 의심하고 동정시험으로 확인한다. 집락이 없거나 또는 동정시험에서 음성으로 판정될 때 검체는 이 시험에 적합하다.
마) 황색포도상구균
① 검액조제 및 전배양 검체 1 g 이상을 취하여 「생균수시험」에 따라 조제한 10 배 희석액의 10 mL 혹은 1 g 또는 1 mL에 해당하는 양을 적당량 (3) 라) 시험법의 적합성에서 결정)의 대두카제인소화액체배지에 접종하여 섞은 다음 30 ∼ 35 ℃에서 18 ∼ 24 시간 배양한다. 경피흡수패취를 시험할 때는 「생균수시험」의 4) 마)①항에 따라 조제한 1 패취 해당량을 멸균멤브레인필터로 여과하고 이 멤브레인필터를 100 mL의 대두카제인소화액체배지 중에 넣는다.
② 선택배양 만니톨염화나트륨한천배지에 이식하고 30 ∼ 35 ℃에서 18 ∼ 72 시간 배양한다.
③ 판정 노란색의 띠로 둘러싼 노란색 또는 흰색집락의 증식이 인정될 때 양성으로 의심하고 동정시험으로 확인한다. 위와 같은 종류의 집락이 없거나 또는 동정시험에서 음성으로 판정될 때 검체는 이 시험에 적합하다.
바) 클로스트리디아
① 검액 조제 및 가열처리 검체 2 g 또는 2 mL 이상을 취하여 「생균수시험」에 따라 10 배 희석액 (최소 20 mL 이상)을 조제한다. 조제한 검액을 최소 10 mL씩 2 개로 나눈다. 그 중 1 개는 80 ℃에서 10 분간 가열한 다음 빨리 식히고 다른 1 개는 가열하지 않는다.
② 선택배양 각각에서 10 mL 또는 검체 1 g 또는 1 mL에 해당하는 양을 적당량 (3) 라) 시험법의 적합성에서 결정)의 강화클로스트리디아배지에 접종하여 섞은 다음 혐기적 조건으로 30 ∼ 35 ℃에서 48 시간 배양한다. 배양 후 각 용기로부터 콜롬비아한천배지로 이식하고 혐기적 조건으로 30 ∼ 35 ℃에서 48 시간 배양한다.
③ 판정 카타라제반응양성의 간균 (아포가 있거나 또는 없는)의 혐기적 증식이 인정되는 경우 양성을 나타내며 동정시험으로 확인한다. 위와 같은 종류의 집락이 없거나 또는 동정시험에서 음성으로 판정될 때 검체는 이 시험에 적합하다.
사) 칸디다알비칸스
① 검체 조제 및 전배양 검체를 「생균수시험」에 따라 조제한다. 그 10 mL 혹은 검체 1 g 또는 1 mL 이상에 해당하는 양을 100 mL의 사부로포도당액체배지에 접종하여 섞어 30 ∼ 35 ℃에서 3 ∼ 5 일간 배양한다.
② 선택배양 사부로포도당한천배지에 이식하고 30 ∼ 35 ℃에서 24 ∼ 48 시간 배양한다.
③ 판정 흰색집락의 증식이 인정될 때에는 양성으로 의심하고 동정시험으로 확인한다. 흰색집락이 없거나 또는 동정시험에서 음성으로 판정될 때 검체는 이 시험에 적합하다.
아래 항은 정보제공을 목적으로 기재한 것이다.
5) 권장 용액 및 배지 아래의 용액 및 배지는 약전의 미생물시험에 규정되어 있는 목적에 적합한 것이다. 적합성이 확인되면 다른 배지를 써도 된다.
보존완충액 인산이수소칼륨 34 g을 물 500 mL에 녹이고 수산화나트륨시액으로 pH 7.0 ∼ 7.4로 조정한 다음 물을 넣어 1000 mL로 하여 섞는다. 용기에 분주하여 멸균한다. 2 ∼ 8 ℃에서 보존한다.
인산완충액, pH 7.2 물과 보존완충액을 혼합 (800 : 1)하여 조제하고 멸균한다.
펩톤염화나트륨완충액, pH 7.0 (Buffered Sodium Chloride-Pepton Solution pH 7.0)
인산이수소칼륨 3.6 g
인산수소이나트륨이수화물 7.2 g (인산염 0.067 mol/L에 상당한다)
염화나트륨 4.3 g
펩톤 (육제 또는 카제인제) 1.0 g
물 1000 mL
검증된 주기로 고압증기멸균한다.
대두카제인소화액체배지 (Soybean-Casein Digest Broth)
카제인제 펩톤 17.0 g
대두제 펩톤 3.0 g
염화나트륨 5.0 g
인산수소이칼륨 2.5 g
포도당 일수화물 2.5 g
물 1000 mL
멸균한 다음의 pH가 25 ℃에서 7.1 ∼ 7.5가 되도록 pH를 조정한다. 검증된 주기로 고압증기멸균한다.
대두카제인소화한천배지 (Soybean-Casein Digest Agar)
카제인제 펩톤 15.0 g
대두제 펩톤 5.0 g
염화나트륨 5.0 g
한천 15.0 g
물 1000 mL
멸균한 다음의 pH가 25 ℃에서 7.1 ∼ 7.5가 되도록 pH를 조절한다. 검증 된 주기로 고압에 증기멸균한다.
사부로포도당한천배지 (Sabouraud Dextrose Agar)
포도당 40.0 g
펩톤 (육제 및 카제인제 1 : 1) 10.0 g
한천 15.0 g
물 1000 mL
멸균한 다음의 pH가 25 ℃에서 5.4 ∼ 5.8이 되도록 pH를 조절한다. 검증된 주기로 고압증기멸균한다.
감자덱스트로스한천배지 (Potato Dextrose Agar)
감자침출액 200 g
포도당 20.0 g
한천 15.0 g
물 1000 mL
멸균한 다음의 pH가 25 ℃에서 5.4 ∼ 5.8이 되도록 pH를 조절한다. 검증된 주기로 고압증기멸균한다.
사부로포도당액체배지 (Sabouraud Dextrose Broth)
포도당 20.0 g
펩톤 (육제 및 카제인제 1 : 1) 10.0 g
물 1000 mL
멸균한 다음의 pH가 25 ℃에서 5.4 ∼ 5.8이 되도록 pH를 조절한다. 검증된 주기로 고압증기멸균한다.
모젤장내세균증균액체배지 (Enterobacteria Enrichment Broth Mossel)
젤라틴제 펩톤 10.0 g
포도당일수화물 5.0 g
건조소담즙 20.0 g
인산이수소칼륨 2.0 g
인산수소이나트륨이수화물 8.0 g
브릴리안트그린 15 mg
물 1000 mL
멸균한 다음의 pH가 25 ℃에서 7.0 ∼ 7.4가 되도록 pH를 조절한다. 100 ℃에서 30 분간 가열하고 바로 식힌다.
바이올렛·레드·담즙산염·포도당한천배지 (Violet Red Bile Glucose Agar)
효모엑스 3.0 g
젤라틴제 펩톤 7.0 g
담즙산염 1.5 g
염화나트륨 5.0 g
포도당일수화물 10.0 g
한천 15.0 g
뉴트랄레드 30 mg
크리스탈바이올렛 2 mg
물 1000 mL
멸균한 다음의 pH가 25 ℃에서 7.2 ∼ 7.6이 되도록 pH를 조절한다. 끓을 때까지 가열한다. 고압증기멸균기로 가열해서는 안 된다.
맥콘키액체배지 (MacConkey Broth)
젤라틴제 펩톤 20.0 g
유당일수화물 10.0 g
건조소담즙 5.0 g
브로모크레솔퍼플 10 mg
물 1000 mL
멸균한 다음의 pH가 25 ℃에서 7.1 ∼ 7.5가 되도록 pH를 조정한다. 검증된 주기에서 고압증기멸균한다.
맥콘키한천배지 (MacConkey Agar)
젤라틴제 펩톤 17.0 g
펩톤 (육제 및 카제인제) 3.0 g
유당일수화물 10.0 g
염화나트륨 5.0 g
담즙산염 1.5 g
한천 13.5 g
뉴트랄레드 30 mg
크리스탈바이올렛 1 mg
물 1000 mL
멸균한 다음의 pH가 25 ℃에서 6.9 ∼ 7.3이 되도록 pH를 조정한다. 끊임없이 저어 섞으면서 1 분간 끓이고 검증된 주기에서 고압증기멸균한다.
라파포트바시리아디스살모넬라증균액체배지 (Rappaport Vassilliadis Salmonella Enrichment Broth)
대두제 펩톤 4.5 g
염화마그네슘육수화물 29.0 g
염화나트륨 8.0 g
인산수소이칼륨 0.4 g
인산이수소칼륨 0.6 g
말라키트그린 36 mg
물 1000 mL
약간 가온하면서 녹이고 115 ℃를 넘지 않는 온도에서 검증된 주기로 고압증기멸균한다. 가열 및 고압증기멸균한 다음의 pH가 25 ℃에서 5.0 ∼ 5.4가 되도록 한다.
엑스엘디한천배지 (Xylose Lysine Deoxycholate Agar, XLD Agar)
자일로스 3.5 g
L-라이신 5.0 g
유당일수화물 7.5 g
백당 7.5 g
염화나트륨 5.0 g
효모엑스 3.0 g
페놀레드 80 mg
한천 13.5 g
데스옥시콜산나트륨 2.5 g
티오황산나트륨오수화물 6.8 g
시트르산암모늄철(II) 0.8 g
물 1000 mL
가열한 다음의 pH가 25 ℃에서 7.2 ∼ 7.6이 되도록 pH를 조정한다. 끓을 때까지 가열하고 50 ℃까지 식힌 다음 페트리접시에 붓는다. 고압증기멸균기로 가열해서는 안 된다.
세트리미드한천배지(Cetrimide Agar)
젤라틴제 펩톤 20.0 g
염화마그네슘육수화물 1.4 g
황산칼륨 10.0 g
세트리미드 0.3 g
한천 13.6 g
물 1000 mL
글리세린 10.0 mL
흔들어 섞으면서 가열하여 1 분간 끓인다. 멸균한 다음의 pH가 25 ℃에서 7.0 ∼ 7.4가 되도록 pH를 조정한다. 검증된 주기로 고압증기멸균한다.
만니톨염화나트륨한천배지 (Mannitol Salt Agar)
카제인제 펩톤 5.0 g
육제 펩톤 5.0 g
육엑스 1.0 g
D-만니톨 10.0 g
염화나트륨 75.0 g
한천 15.0 g
페놀레드 25 mg
물 1000 mL
흔들어 섞으면서 가열하여 1 분간 끓인다. 멸균한 다음의 pH가 25 ℃에서 7.2 ∼ 7.6이 되도록 pH를 조정한다. 검증된 주기로 고압증기멸균한다.
강화클로스트리디아배지 (Reinforced Medium for Clostridia)
육엑스 10.0 g
펩톤 10.0 g
효모엑스 3.0 g
용성전분 1.0 g
포도당일수화물 5.0 g
시스테인염산염 0.5 g
염화나트륨 5.0 g
아세트산나트륨 3.0 g
한천 0.5 g
물 1000 mL
한천을 물에 넣어 계속 저으면서 끓을 때까지 가열하여 녹인다. 필요하면 멸균한 다음의 pH가 25 ℃에서 약 6.6 ∼ 7.0이 되도록 pH를 조정한다. 검증된 주기로 고압증기멸균한다.
콜롬비아한천배지 (Columbia Agar)
카제인제 펩톤 10.0 g
육침출물의 펩신소화물 5.0 g
심근침출물의 판크레아틴소화물 3.0 g
효모엑스 5.0 g
옥수수전분 1.0 g
염화나트륨 5.0 g
한천 (겔강도에 따라) 10.0 ~ 15.0 g
물 1000 mL
한천을 물에 넣어 계속 저으면서 끓을 때까지 가열하여 녹인다. 필요하면 멸균한 다음의 pH가 25 ℃에서 7.1 ∼ 7.5가 되도록 pH를 조정한다. 검증된 주기로 고압증기멸균한다. 45 ∼ 50 ℃로 식힌 다음 필요에 따라 겐타마이신염기 20 mg에 상당하는 양의 겐타마이신황산염을 넣어 페트리접시에 부어 넣는다.
9. 박층크로마토그래프법
박층크로마토그래프법은 실리카겔로 만든 박층판을 써서 혼합물을 성분의 물리적 및 화학적성질의 차이를 이용하여 전개용매로 전개할 때 각각의 성분으로 분리하여 확인하는 방법이다.
장 치 실리카겔박층판 (평활한 내열성의 유리판(세로 200 mm, 가로 50 mm 또는 200 mm, 두께 3 mm) 위에 적당한 장치를 써서 실리카겔(박층크로마토그래프용)을 두께 250 μm 이상 300 μm이하의 박층 상태로 균일하게 도포하고 박층을 위로하여 수평으로 놓고 실온에서 2 시간 ∼ 3 시간 바람에 말린 다음 105 ℃에서 1 시간 가열한 다음 건조제를 넣은 기밀용기에서 냉각하여 만든 것에 한함.) 및 전개용 용기(실리카겔박층판을 내부에 똑바로 세우고 밀폐한다)
조 작 법 제 1 법 박층판의 아래끝에서 약 20 mm 높이의 위치를 원선으로 하고 좌우 양측에서 적어도 10 mm를 띄어서 원선 위에 각조에서 규정하는 양의 검액 및 표준액을 마이크로피펫 등을 써서 약 10 mm 이상의 적당한 간격으로 점적하고 바람에 말린다. 각조에서 규정하는 전개용매를 약 10 mm의 깊이로 넣고 포화시킨 전개용 용기에 박층판을 기벽에 닿지 않도록 넣고 용기를 밀폐하여 상온에서 전개한다. 다음에 전개용매를 선단으로부터 원선까지 약 100 mm의 거리까지 전개하였을 때 박층판을 꺼내어 곧 용매의 선단의 위치를 표시하고 바람에 말린 다음 검액 및 표준액으로부터 얻은 주반점의 위치 색 등을 비교한다. 이 경우에 값은 다음의 식에 따라 구한다.
제 2 법 제 1 법에 따라 시험하고 다음 식에 따라 값을 구한다.
10. 불꽃반응시험법
불꽃반응시험법은 검체를 염산으로 적시고 불꽃 속에서 그 불꽃의 색을 관찰하여 구조 중 존재하는 칼륨염, 나트륨염, 칼슘염을 확인하는 시험법이다.
조 작 법 검체 0.1 g에 염산 0.2 mL를 넣어 이상 (泥狀)으로 만들고 그 소량을 백금선의 끝에서 약 5 mm 부분까지 묻혀 무색 불꽃 속에 수평으로 넣어 불꽃의 색을 관찰한다. 이 경우에 칼륨염, 나트륨염, 칼슘염이 나타내는 불꽃의 색은 각각 다음과 같다.
1) 칼륨염 엷은 보라색
2) 나트륨염 황색
3) 칼슘염 황적색
4) 바륨염 황록색
5) 스트론튬염 진한 홍색
11. 불소시험법
불소시험법은 검체중에 함유되는 불소의 양의 한도를 시험하는 방법이다. 그 한도는 불소(F)의 중량백분율(%)로 표시한다.
장 치 그림과 같은 장치를 쓴다.
A : 증류플라스크(용량 약 300㎖)
B : 수증기발생기(용량 약 1ℓ)
C : 냉각기
D : 수기(용량 약 200㎖)
E : 수증기 도입관(안지름 약 8㎜)
F : 핀치콕크가 달린 고무관
G : 온도계
조 작 법
1) 검액의 조제 불소 100~300㎍에 해당 하는 양의 검체를 정밀하게 달아 물 20~30㎖를 써서 증류플라스크 A에 씻어 넣고 유리구슬 8~12개, 희석시킨 정제황산 50㎖ 및 검체중의 염소이온에 해당하는 양 이상으로 황산은을 넣어 섞는다. 다음 A를 미리 수증기 도입관 E에 수증기를 통해서 씻은 증류장치에 연결한다. 수기 D에는 물 약 20㎖를 넣고 냉각기 C의 끝을 이 물에 잠기게 한다. A를 가열하여 액의 온도가 130℃로 될 때 핀치콕크로 고무관 F를 막고 수증기발생기 B에서 수증기를 통한다. 동시에 A액의 온도를 140±5℃로 유지하도록 가열을 조절한다. 유액이 170~180㎖가 되었을 때 증류를 그치고 유액을 메스플라스크에 옮겨 D를 물 소량으로 씻고 씻은 액을 유액에 합하고 물을 넣어 200㎖로 하여 검액으로 한다.
2) 정량조작 검액 및 불소표준액 20㎖씩을 각각 50㎖ 메스플라스크에 넣고 불소시험법용 알리자린콤플렉손시액 1㎖, 질산란탄시액 1㎖, pH 5.2 초산․초산나트륨완충액 5㎖, 아세톤 20㎖ 및 물을 넣어 50㎖로 하고 잘 섞어 1시간 방치한 다음 파장 620㎚에서 흡광도를 측정한다. 따로 물 20㎖를 50㎖ 메스플라스크에 취하고 검액의 조제와 같은 방법으로 조작하여 대조액으로 한다.
A : 검액에서 얻은 정색도의 흡광도
AS : 불소표준액에서 얻은 정색도의 흡광도
12. 불용물시험법
불용물시험법은 검체 중에 함유되어 있는 물 또는 유기용매에 녹지 않는 물질의 양을 시험하는 방법으로 그 양을 질량백분율 (%)로 나타낸다.
조 작 법 제 1 법 따로 규정이 없는 한 검체 약 2 g을 정밀하게 달아 열탕 200 mL를 넣어 진탕 혼화한 다음 실온에서 식힌다. 질량을 아는 도가니형 유리여과기(1G4)로 여과한 다음 잔류물을 씻은 액이 무색을 나타낼 때까지 물로 씻은 다음 도가니형 유리여과기를 105 ℃에서 3시간 건조한다. 건조한 다음 데시케이터 (실리카겔) 속에서 방치하여 식힌 다음 질량을 정밀하게 단다.
제 2 법 검체 약 0.2 g ∼ 0.5 g 을 정밀하게 달아 각조에 규정된 용매 100 mL를 넣어 혼합하고 냉각기를 달아 20 분간 끓인다. 질량을 아는 도가니형 유리여과기(1G4)로 뜨거울 때 여과한 다음 불용물을 온용매 10 mL씩으로 씻은 액이 무색을 나타낼 때까지 씻는다. 다음 도가니형 유리여과기를 105 ℃에서 3 시간 건조한다. 건조한 다음 데시케이터 (실리카겔) 속에서 방치하여 식힌 다음 질량을 정밀하게 단다.
13. 비소시험법
비소시험법은 색소 중에 혼재하는 비소의 한도시험이다. 그 한도는 삼산화비소 (As2O3)의 양으로 나타낸다. 각조에서는 비소 (As2O3로서)의 한도를 ppm으로 ( ) 안에 나타낸다.
장 치 그림과 같은 장치를 쓴다. 배기관 B에 약 30 mm의 높이로 유리섬유 F를 채우고 아세트산납시액ㆍ물혼합액(1 : 1)으로 고르게 적신 다음 밑에서 약하게 흡인하여 과량의 액을 제거한다. 이것을 고무마개 H의 중심에 수직으로 끼우고 B의 아래에 있는 작은 구멍 E는 고무마개 아래까지 약간 내려가도록 하여 발생병 A에 끼운다. B의 위쪽 끝에는 유리관 C를 수직으로 고정시킨 고무마개 I를 끼운다. C의 배기관측의 아래쪽 끝은 고무마개 I의 아래쪽 끝과 같은 평면이 되도록 한다.
* 숫자는 mm를 표시
A : 발생병 (어깨 부분까지의 내용량 약 70 mL, 40 mL에 표선이 있다.)
B : 배기관
C : 유리관 (안지름 5.6 mm, 흡수관에 넣는 부분은 끝을 안지름 1 mm로 잡아 늘인다)
D : 흡수관 (안지름 10 mm) E : 작은 구멍 F : 유리섬유 (약 0.2 g)
G : 5 mL의 표선 H 및 I : 고무마개
검액의 조제법 검체 약 1.0 g을 달아 백금제, 석영제 또는 사기제 도가니에 넣는다. 여기에 질산마그네슘의 에탄올용액(1 → 50) 10 mL를 넣어 에탄올에 점화하여 연소시킨 다음 천천히 가열하고 강열하여 회화시킨다. 만일 이 방법으로 탄화물이 남아있을 때는 소량의 질산으로 적시고 천천히 가열한 다음 강열하여 회화시킨다. 식힌 다음 잔류물에 염산 3 mL를 넣고 필요하면 물 약 10 mL를 넣어 수욕에서 가온하여 녹여 검액으로 한다.
조 작 법 표준색의 조제는 동시에 한다. 발생병 A에 검액을 취하여 메틸오렌지시액 1 방울을 넣고 암모니아시액, 강암모니아수을 써서 중화시킨 다음 희석시킨 염산(1 → 2) 5 mL 및 요오드화칼륨시액 5 mL를 넣어 2 ∼ 3 분간 방치한 다음 산성염화제일석시액 5 mL를 넣고 실온에서 10 분간 방치한다. 다음에 물을 넣어 40 mL로 하고 비소분석용 아연 2 g을 넣고 곧 B 및 C를 연결한 고무마개 H를 발생병 A에 끼운다. C의 세관부 끝은 미리 비화수소흡수액 5 mL를 넣은 흡수관 D의 밑에까지 닿도록 넣어 둔다. 다음에 발생병 A를 25 ℃의 물속에 어깨까지 잠기게 넣어 1 시간 방치한다. 흡수관을 꺼내고 필요하면 피리딘을 넣어 5 mL로 하고 흡수액의 색을 관찰한다. 이 색은 표준색보다 진하지 않다.
표준색의 조제 발생병 A에 비소표준액 2 mL를 정확하게 넣고 다시 희석시킨 염산(1 → 2) 5 mL 및 요오드화칼륨시액 5 mL를 넣어 2 ∼ 3 분간 방치한 다음 산성염화제일석시액 5 mL를 넣고 실온에서 10 분간 방치한다. 이하 앞에서와 같은 방법으로 조작하여 얻은 흡수액의 정색을 표준색으로 한다. 이 색은 삼산화비소 (As2O3) 2 μg에 해당한다.
※ 주의 시험에 쓰는 기구, 시약 및 시액은 비소를 함유하지 않거나 거의 함유하지 않은 것을 쓰고 필요하면 공시험을 한다.
14. 비중측정법
비중 라 함은 검체와 물과의 각각 t'℃ 및 t℃에 있어서 같은 체적의 중량비를 말한다. 다음 제1법, 제2법 또는 제3법에 따라 측정한다.
조 작 법
제1법
1) 비중병에 의한 측정법 비중병은 보통 내용 10~100㎖의 유리용기로 온도계가 붙은 갈아 맞춘 마개 및 표선과 갈아 맞춘 뚜껑이 있는 측관 등이 있다. 미리 깨끗이 씻고 건조한 비중병의 무게 W를 정밀하게 단다. 다음 마개 및 뚜껑을 열어 검체를 채우고 t'℃보다 1~3℃ 낮게 하고 기포가 없게 뚜껑을 잘 닫는다. 천천히 온도를 올려 온도계가 t'℃를 나타낼 때 표선의 윗쪽의 검체를 측관에서 빼내고 측관에 뚜껑을 닫고 바깥쪽을 잘 닦은 다음 무게 W1를 정밀하게 단다. 다시 같은 비중병으로 물을 써서 같은 조작을 하고 t℃에 있어서의 무게 W2를 정밀하게 단다.
2) 쉬프렝겔․오스트발트비중병에 의한 측정법 쉬프렝겔․오스트발트비중병은 보통 내용 1~10㎖의 유리용기로 그림과 같이 양쪽 끝이 두꺼운 세관(細管)으로 되어 한쪽세관 A에는 표선 C가 있다. 미리 깨끗이 닦아 건조한 피크노메타를 백금 또는 알루미늄 등의 선 D로 화학천칭의 저울대의 고리에 걸어서 무게를 단다. 다음 t'℃보다 3~5℃ 낮은 검체중에 세관 B를 담근다. A에는 고무관 또는 갈아맞춘 세관을 붙여 거품이 들어가지 않게 조심하면서 검체를 C위까지 빨아 올린다. 다음 t'℃의 수욕중에 약 15분간 담근 다음 B의 끝에 여과지편을 대어 검체의 끝을 C에 일치시킨다.
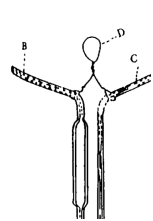
수욕중에서 들어 내어 바깥쪽을 잘 씻고 무게 W1를 달고 같은 피크노메타를 써서 물로 같은 방법으로 조작하여 그 t℃에서의 무게 W2를 칭량한다. 1)의 식에 따라 비중를 구한다.
3) 비중부액계에 의한 측정법 규정온도용의 비중부액계로 필요한 정밀도를 갖는 것을 쓴다. 비중부액계는 에탄올 또는 에텔로 깨끗이 씻은 것을 쓴다. 검체를 잘 흔들어 섞은 다음 거품이 없어지면 비중부액계를 띄운다. 규정온도에서 비중부액계가 정지했을 때 메니스커스의 상연에서 비중의 눈금을 읽는다. 다만 눈금 읽는 방법이 표시되어 있는 비중부액계는 그 방법을 따른다.
제2법 제1법의 1)에서 쓴 비중병과 같은 형의 25㎖ 비중병에 등유(燈油)를 약 6㎜의 깊이로 넣고 그 무게 W를 정밀하게 달아 여기에 원료각조의 건조감량항에서 규정하는 조건으로 건조한 검체 1~2㎖를 넣어 그 무게 W1를 정밀하게 단다. 등유를 써서 기벽에 부착한 검체를 비중병에 씻어 넣고 등유를 추가하여 검체를 덮는다. 비중병을 데시케이터에 넣고 3㎜Hg이하로 감압하여 거품이 생기지 않게 되었을 때 비중병을 꺼내어 등유를 가득 채운다. 이것을 17~19℃로 하고 천천히 온도를 올려 온도계가 20℃로 되었을 때 표선 윗쪽의 등유를 측관으로 부터 빼내고 측관에 마개를 한 다음 겉을 닦은 다음 무게 W2를 정밀하게 단다. 다시 같은 비중병에 등유를 넣어 앞에서와 같은 조작을 하여 20℃에서의 무게 W3를 정밀하게 단다.
제3법 미리 제1법의 1)에서 쓴 비중병과 같은 형의 비중병의 무게 W를 정밀하게 단 다음 마개 및 뚜껑을 빼고 융해한 검체가 온도계 끝에 닿지 않게 검체를 넣고 온도계를 삽입치 않고 천천히 온도를 올려 검체의 융해온도보다 약간 높은 온도로 1시간 유지하여 검체중의 거품을 제거한다. 식힌 다음 온도계 및 뚜껑을 하고 무게 W1를 정밀하게 단다. 다음에 마개 및 뚜껑을 빼고 검체위에 물을 채우고 20℃보다 1~3℃ 낮게하여 거품이 남지 않게 조심하면서 마개를 한다. 천천히 온도를 올려 온도계가 20℃로 되었을 때 표선 위의 물을 측관으로 부터 빼내어 측관에 뚜껑을 닫고 겉을 닦은 다음 무게 W2를 정밀하게 단다. 다시 같은 비중병에 물을 넣어 앞에서와 같은 조작을 하여 20℃에서의 무게 W3를 정밀하게 단다.
15. 산가용물시험법
산가용물시험법은 검체중의 묽은염산에 녹는 물질의 양을 측정하는 방법이다.
조 작 법 따로 규정이 없는 한 검체 약 1g을 정밀하게 달아 묽은염산 20㎖를 넣어 50℃에서 15분간 저어 섞으면서 가온한 다음 물을 넣어 정확하게 50㎖로 하여 여과한다. 처음 여액 15㎖를 버리고 다음 여액 25㎖를 정확하게 취하여 수욕상에서 증발건고하여 항량이 될 때까지 강열하고 데시케이터(실리카 겔)속에서 방냉한 다음 그 무게를 정밀하게 단다.
16. 산불용물시험법
산불용물시험법은 검체중의 염산에 녹지 않는 물질의 양을 측정하는 방법이다.
조 작 법 따로 규정이 없는 한 원료각조에서 규정한 검체의 양을 정밀하게 달아 물 약 70㎖를 넣어 저어 섞으면서 염산 10㎖를 조금씩 넣어 5분간 끓인다. 식힌 다음 정량분석용여과지(5종C)를 써서 여과하고 여과지위의 잔류물을 열탕으로 씻고 씻은 액에 질산은시액으로 염화물의 반응이 나타나지 않을 때 잔류물을 여과지와 함께 회화하여 항량이 될 때까지 강열하고 데시케이터(실리카 겔)속에서 식힌 다음 그 무게를 정밀하게 단다.
17. 색소시험법
가. 물불용물
검체 2g에 열탕 200mL를 가하여 잘 흔들어 섞은 다음 방냉하고 불용물을 미리 무게를 단 도가니형 유리여과기(1G4)로 여과하여 씻은 액이 무색이 될 때까지 물로 씻고 유리여과기와 같이 135℃에서 3시간 건조한 다음 데시케이타에서 식히고 평량한다.
나. 염화물 및 황산염
검체 약 0.1g을 정밀히 달아 물을 가하여 녹이고 정확히 100mL로 한 것을 시험용액으로 한다. 별도로 500∼600℃에서 1시간 건조한 염화나트륨(표준시약) 0.165g을 정밀히 달아 물을 가하여 녹여 1,000mL로 한 것을 염화물이온표준원액으로 한다. 또한 100℃에서 2시간 건조한 황산나트륨 0.148g을 정밀히 달아 물을 가하여 녹여 1,000mL로 한 것을 황산이온표준원액으로 한다. 이 염화물이온 및 황산이온의 표준원액 각각 0.2mL, 1mL, 10mL 및 50mL를 취하여 각각에 물을 가하여 정확히 100mL로 한 것을 표준용액으로 한다. 시험용액 및 표준용액 각각 20μL 취하여 다음의 조작조건으로 이온크로마토그래피을 행한다. 먼저 각각의 표준용액의 염화물이온 및 황산이온의 피크면적을 측정하여 검량선을 작성한 후 시험용액의 염화물이온 및 황산이온의 피크면적을 측정하여 검량선으로부터 각각의 이온량을 구하고, 여기에서 얻어진 이온량에 염화물이온은 1.65, 황산이온은 1.48을 곱하여 시험용액 중 염화나트륨 및 황산나트륨의 농도를 구하여 검체 중 함량을 산출한다.
< 조작조건 >
검 출 기 : 전기전도도검출기
칼럼충진제 : 전다공성음이온교환체
칼 럼 : 내경 2∼4mm, 길이 20∼25cm의 스테인레스관 또는 플라스틱관
용 리 액 : 1.8mM 탄산나트륨용액
1.7mM 탄산수소나트륨용액
유 속 : 1.0∼1.5mL/min
다. 비 소
검체 0.5g을 백금제, 석영제 또는 자제도가니에 취하여 질산마그네슘의 에탄올용액(1→50) 20mL를 넣고 에탄올에 점화하여 연소시킨 다음 서서히 가열하여 450∼550℃로 회화한다.
만일 탄화물이 존재하면 소량의 질산으로 적신 다음 다시 강열하고 450∼550℃로 회화한다.
식힌 다음 잔류물에 염산 6mL를 가하고 필요하면 물 약 10mL를 가하여 수욕상에서 가온하여 냉각시킨 후 물을 가하여 25mL로 한 것을 시험용액으로 하여 비소시험법에 따라 시험할 때, 이에 적합하여야 한다. 다만, 표준색은 비소표준용액 2mL를 취하여 검체의 경우와 같이 처리하여 만든다(4ppm 이하).
라. 중 금 속
검체 2.5g을 취하여 강열잔류물시험법과 같이 처리하여 완전히 회화시키고 이에 염산 3mL를 가하여 저어 섞고, 다시 물 7mL를 가하여 흔들어 섞은 다음 정량분석용여과지(5종C)로 여과한다. 여과지상의 잔류물을 묽은염산 5mL 및 물 5mL로 씻고 그 씻은 액을 여액에 합쳐 A액으로 하고 이에 물을 가하여 50mL로 한 액을 시험용액으로 한다. 다만, 크롬 및 망간을 시험할 경우에는 다음 조작을 추가한다. 앞의 여과지상의 잔류물을 여과지와 같이 105℃에서 건조한 다음, 백금도가니에 넣어 약 450℃로 가열하여 회화시킨다. 이에 무수탄산나트륨 1∼2g을 가하여 마개를 덮고 가열하여 녹인다.
식힌 다음 물 10mL를 가하고 염산 3∼6mL를 적가하여 산성으로 한 다음, 이를 소량의 물을 써서 비이커에 옮기고 세게 저어 섞은 다음 A액과 합치고 물을 가하여 50mL로 하여 시험용액으로 한다. 따로 검체를 쓰지 아니하고 검체의 경우와 같이 처리하여 공시험용액을 만든다.
(1) 아 연 : 시험용액 2.5mL에 염산(1→4) 10mL 및 물을 가하여 50mL로 한 액을 B액으로 한다. 따로, 공시험용액 2.5mL에 아연표준용액 2.5mL, 염산(1→4) 10mL 및 물을 가하여 50mL로 한 액을 대조액으로 한다. B액 및 대조액을 다음의 조작조건으로 원자흡광광도법에 따라 시험할 때, B액의 흡광도는 대조액의 흡광도보다 높아서는 아니 된다(200ppm 이하).
< 조작조건 >
가연성가스 : 아세틸렌
조연성가스 : 공 기
램 프 : 아연중공음극램프
파 장 : 213.9nm
(2) 크 롬 : 따로 규정이 없는 한, 시험용액 10mL에 염산(1→4) 10mL 및 물을 가하여 50mL로 한 액을 C액으로 한다. 따로, 공시험용액 10mL에 크롬표준용액 10mL, 염산(1→4) 10mL 및 물을 가하여 50mL로 한 액을 대조액으로 한다. C액 및 대조액을 다음의 조작조건으로 원자흡광광도법에 따라 시험할 때, C액의 흡광도는 대조액의 흡광도보다 높아서는 아니 된다(50ppm 이하).
< 조작조건 >
가연성가스 : 아세틸렌
조연성가스 : 공기
램 프 : 크롬중공음극램프
파 장 : 357.9nm
(3) 철 : 시험용액 2mL에 염산(1→4) 10mL 및 물을 가하여 50mL로 한 액을 D액으로 한다. 따로, 공시험용액 2mL에 철표준용액 5mL, 염산(1→4) 10mL 및 물을 가하여 50mL로 한 액을 대조액으로 한다. D액 및 대조액을 다음의 조작조건으로 원자흡광광도법에 따라 시험할 때, D액의 흡광도는 대조액의 흡광도보다 높아서는 아니 된다(500ppm 이하).
< 조작조건 >
가연성가스 : 아세틸렌
조연성가스 : 공기
램 프 : 철중공음극램프
파 장 : 248.3nm
(4) 망 간 : 따로 규정이 없는 한, 시험용액 4mL에 염산(1→4) 10mL 및 물을 가하여 50mL로 한 액을 E액으로 한다. 따로, 공시험용액 4mL에 망간표준용액 1mL, 염산(1→4) 10mL 및 물을 가하여 50mL로 한 액을 대조액으로 한다. E액 및 대조액을 다음의 조작조건으로 원자흡광광도법에 따라 시험할 때, E액의 흡광도는 대조액의 흡광도보다 높아서는 아니 된다(50ppm 이하).
< 조작조건 >
가연성가스 : 아세틸렌
조연성가스 : 공기
램 프 : 망간중공음극램프
파 장 : 279.5nm
(5) 기타의 중금속 : A액에 물을 가하여 50mL로 한다. 이 액 20mL를 취하여 네슬러관에 넣고 페놀프탈레인시액 1방울을 가하여 액이 홍색을 나타날 때까지 암모니아시액을 가한 다음, 초산(1→4) 2mL를 가하고 필요시 여과한다. 여과지를 물로 씻은 다음 물을 가하여 50mL로 한 것을 H액으로 한다.
따로 공시험용액 20mL를 정량하여 네슬러관에 넣고 납표준용액 2.0mL 및 페놀프탈레인시액 1방울을 가하여 H액과 마찬가지로 조작한 것을 I액으로 한다.
양 액에 황화나트륨시액을 2방울씩을 가하여 흔들어 섞고 5분간 방치할 때, H액의 색은 I액의 색보다 진해서는 아니 된다(20ppm 이하).
마. 부성색소
표준원액 5.0mL, 2.0mL 및 1.0mL을 달아 초산암모늄 액을 가하여 각각 정확히 100mL로 한 것을 표준용액으로 한다. 시험용액 및 표준용액 각각 20μL씩을 취하여 아래의 조작조건으로 액체크로마토그래피를 하여 시험용액의 부성색소의 피크면적을 측정하고 검량선으로 부터 각각의 색소량을 구하여 그 합계치를 구한다.
조작조건
검출기 : 가시부흡수검출기
칼 럼 : 5μm의 화학결합형 C18칼럼(내경 4∼6mm, 길이 15∼30cm) 또는 이와 동등한 것
유 속 : 1mL/min
측정파장 : 515nm
이 동 상 : A : 초산암모늄용액(7.7→1,000)
B : 아세토니트릴 : 메탄올(70 : 30)
A액 : B액(100 : 0)→A액 : B액(30 : 70) 25분
바. 미반응원료 및 반응중간체
표준원액 5.0mL, 2.0mL 및 1.0mL을 달아 따로 초산암모늄 용액을 가하여 각각 정확히 100mL로 한 것을 표준용액으로 한다. 시험용액 및 표준용액 각각 20μL씩을 달아 각각의 액에 대하여 아래의 조작조건으로 액체크로마토그래피를 하여 시험용액의 미반응원료 및 반응중간체의 피크면적을 측정하여, 검량선으로부터 그 양을 구한다.
조작조건
검 출 기 : 자외부흡수검출기
칼 럼 : 5μm의 화학결합형 C18칼럼(내경 4∼6mm, 길이 15∼30cm) 또는 이와 동등한 것
유 속 : 1mL/min
측정파장 : 290nm
이 동 상 : A : 초산암모늄용액(7.7→1,000)
B : 아세토니트릴 : 메탄올(70 : 30)
A액 : B액(100 : 0)→A액 : B액(30 : 70) 50분
사. 비술폰화방향족제1급아민
(1) 아닐린으로서
검체 약 2g을 정밀히 달아, 물 l00mL가 들어간 분액깔때기에 넣고 물 50mL를 가하여 녹이고, 수산화나트륨용액(4→100) 5mL 및 초산에틸 50mL를 가하여 흔들어 혼합추출한다. 초산에틸층을 분취한 후 물층에 초산에틸 50mL를 가하여 흔들어 섞고 혼합하여 추출한다. 초산에틸추출액을 합하여 수산화나트륨용액(4→1,000)으로 빛깔이 없어질 때까지 수세한다. 이 초산에틸추출액을 염산(3→10) 10mL로 3회 추출하고 염산추출액을 합하여 물을 가하여 정확히 100mL로 한 것을 A액으로 한다. A액 10mL를 시험관에 넣고 10분간 얼음 속에서 냉각하고 브롬화칼륨용액(1→2) 1mL 및 아질산나트륨용액(1→30) 0.05mL를 가하여 혼합하고 10분간 얼음 속에서 방치한다.
이 혼합액을 0.05mo1/L 3-히드록시-2,7-나프탈렌술폰산이나트륨용액 1mL 및 탄산나트륨용액(1→10) 10mL를 미리 넣은 25mL의 메스플라스크에 옮겨 물을 가하여 정확히 25mL로 하여 15분간 그늘에서 방치하여 시험용액으로 한다.
따로 아닐린 10mg를 달아 염산(3→10) 30mL를 가하여 녹이고, 여기에 물을 가하여 정확히 100mL로 한다. 이 용액 2.0mL를 달아 염산(1→10)을 가하여 100mL로 한다. 이 액을 A액과 마찬가지로 조작하여 비교액으로 하여 흡광도를 측정한다.
시험용액의 경우에는 A액 10mL를 25mL의 메스플라스크에 넣고 0.05mol/L 3-히드록시-2,7-나프탈렌술폰산이나트륨용액 1mL 및 탄산나트륨용액(1→30) 10mL를 가하고 물을 가하여 정확히 25mL로 한 것을 대조액으로 하여 비교액의 경우에는 염산(1→10) 10mL에 0.05mol/L 3히드록시2,7-나프탈렌술폰산이나트륨용액 1mL 및 탄산나트륨용액(1→30) 10mL를 가하고 물을 가하여 정확히 25mL로 한 것을 대조액으로 하여 각각의 액에 대하여 510nm에서 흡광도를 측정할 때 시험용액의 흡광도는 비교액의 흡광도 이하이어야 한다.
아. 정 량 법
(1) 삼염화티탄법
(가) 규정량의 시험용액을 취하여 500mL 삼각플라스크에 넣고 구연산나트륨 15g 및 물을 가하여 약 200mL로 한 다음 이 액 중에 이산화탄소를 통하면서 동시에 세게 끓이면서 0.1N 삼염화티탄용액으로 적정한다. 종말점은 검체의 고유색이 없어진 때로 한다.
(나) 구연산나트륨 대신 주석산수소나트륨 15g을 써서 (가)와 같이 시험한다.
(다) 구연산나트륨 대신 주석산수소나트륨 15g을 써서 (가)와 같이 시험한다.
다만, 지시약으로서 식용색소녹색제2호용액(1→1,000) 10mL를 쓰며 따로 같은 방법으로 공시험을 한다.
(2) 중 량 법
규정량의 시험용액을 취하여 500mL 비이커에 넣고 끓인 다음 염산(1→50) 25mL를 가하여 다시 끓인다. 다음 비이커의 내벽을 물 약 5mL로 씻고 시계접시로 덮어 수욕상에서 약 5시간 가열한 다음 방냉하고, 침전을 미리 무게를 단 유리여과기(1G4)로 여과한 다음 염산(1→200) 10mL씩으로 3회 씻고, 다시 물 약 10mL씩으로 2회 씻는다.
이 침전을 유리여과기와 같이 135℃에서 3시간 건조한 다음 데시케이타에서 식히고 평량한다.
18. 수은시험법
따로 규정이 없는 한, 다음의 어느 한 방법에 따라 측정한다.
가. 환원기화원자흡광광도법
1) 장치
(1) 원자흡광광도계 : 석영제 흡수셀이 부착된 것
(2) 램프 : 수은중공음극램프
(3) 수은 환원기화장치
2) 시액
(1) 염화제일주석용액 : 염화제일주석이수화물(SnCl2ㆍ2H2O) 10g을 1N 황산에 녹여 1,000mL로 한다.
(2) 수은표준용액
염화제이수은 0.135g을 10% 질산 100mL에 녹이고 물을 가하여 1,000mL로 한다. 사용할 때 이 용액을 1% 질산으로 1,000배 희석하여 표준용액으로 한다.
수은표준용액 1mL = 0.1 μg Hg
3) 시험용액의 조제
따로 규정이 없는 한, 검체 5∼10g을 분해플라스크에 넣고 물 10mL 및 질산 20mL를 가하여 천천히 흔들어 준 다음 황산 20mL를 서서히 넣는다. 환류냉각기를 부착하고 갈색의 연기가 발생하지 않을 때까지 분해플라스크를 가열한다. 이 때 분해액이 무색∼담황색의 투명한 액이 되지 않을 때에는 식힌 다음 질산 5mL를 가하고 위의 조작을 반복한다. 식힌 다음 물 50mL 및 10% 요소용액 10mL를 넣고 10분간 끓이고 식힌 후 과망간산칼륨 1g을 넣고 약 10분간 때때로 흔들어 주면서 방치한다. 이 조작을 자홍색이 남을 때까지 반복하고 20분간 끓여 액의 자홍색이 없어지면 식힌 다음 과망간산칼륨 1g을 넣고 다시 20분간 가열한다. 이 때 액의 자홍색이 없어지면 과망간산칼륨의 첨가 및 가열 조작을 다시 2회 되풀이 하고 식혀 용액이 무색 투명하게 될 때까지 20% 염산히드록실아민용액을 주의하면서 가해준다. 식힌 다음 분해액을 다른 플라스크에 옮기고 환류냉각기와 분해플라스크의 내부 및 연결부분을 물로 씻고 세액을 합치고 물로 일정량으로 한 액을 시험용액으로 한다.
수은분해장치의 예
4) 조작법
미리 20%(v/v) 황산농도가 되도록 조절한 시험용액 및 공시험용액 각 100mL를 시험용액병에 취하여 환원기화장치에 연결한 다음 염화제일주석용액 10mL를 가한 즉시 마개를 하고 다이아프램펌프(diaphram pump)로 공기를 흡수셀 중에 순환시켜 파장 253.7nm에서 흡광도를 측정한다. 따로 수은표준용액 1, 5, 10, 15, 20mL에 물을 가하여 각각 100mL로 한 것을 시험용액과 동일한 조작을 한 다음 흡광도를 측정하여 검량선을 작성하고 시험용액의 흡광도를 검량선에 대입하여 수은량을 산출한다.
나. 금아말감원자흡광광도법
1) 장치
시료의 연소에서 금아말감에 의한 포집, 냉원자흡광광도법에 의한 측정까지 자동화된 수은측정장치를 사용한다. 다만, 연소부에 별도의 촉매제가 장착된 수은측정장치를 사용할 수 있다.
2) 시약 및 시액
(1) 수은표준원액 : 염화제이수은 0.135g을 0.001% L-시스테인용액에 녹여 1,000mL로 한다.
수은표준원액 1mL = 100μg Hg
(2) 수은표준용액 : 수은표준원액을 0.001% L-시스테인용액으로 희석하여 0∼200ng/mL로 한다.
(3) 첨가제 : (a) 산화알루미늄 및 (b) 수산화칼슘ㆍ탄산나트륨(1:1)을 사용할 때 950℃에서 30분간 활성화 시킨다.
3) 조작법
첨가제 (a) 약 1g을 도자기제 보트에 고르게 펴고, 그 위에 고체시료의 경우에는 세절하여 균질화한 시료를 10∼300 mg을 취한다. 액체 시료의 경우에는 0.1∼0.5mL를 첨가제 (a)에 완전히 스며들도록 한다. 다시 그 위에 첨가제 (a) 약 0.5g 및 첨가제 (b) 1g을 차례로 고르게 펴 층을 이루게 한다. 다만, 연소부에 별도의 촉매제가 장착된 자동수은분석기의 경우에는 니켈제 보트에 첨가제를 가해주지 않고 시료만을 취한다. 보트를 연소로 안에 넣고 공기 또는 산소를 0.5∼1L/min로 흘려주면서, 약 900℃로 가열하여 수은을 유출하고 포집관에 포집한다. 포집관을 약 700℃로 가열하여, 수은 증기를 냉원자흡광분석장치에 보내고 흡광도를 측정하여 A로 한다. 따로, 도자기제 보트에 첨가제만으로 동일하게 흡광도를 측정하여 Ab로 한다. 따로 수은표준용액을 이용하여 동일하게 조작하여 얻어진 흡광도로부터 검량선을 작성하고, A - Ab 값을 검량선에 대입하여 검체 중 수은량을 산출한다.
19. 염색반응시험법
염색반응의 시험에 쓰이는 백금선은 지름 약 0.8mm의 것으로서 끝은 직선 그대로 사용 한다. 검체가 고체일 때에는 염산 소량을 가하여 죽모양으로 하고 그 소량을 백금선의 끝 약 5mm의 부분에 묻혀 즉시 그림과 같이 거의 수평으로 유지하면서 무색불꽃 중에 넣어 시험한다. 검체가 액체일 때는 백금선의 끝을 검체중에 약 5mm 넣었다가 천천히 꺼내어 고체의 경우와 같이 시험한다. 또한 나트륨염의 칼륨을 시험할 때에는 코발트글라스를 써서 관찰한다. 염색반응이 지속한다란 그 반응이 약 4초간 지속함을 말한다.
20. 염화물시험법
가. 타르색소
염화물시험법은 검체 중에 혼재하는 염화물의 한도시험이다. 그 양은 염화나트륨 (NaCl로서)의 양으로서 한도를 (%) 로 나타낸다.
조 작 법 검체 약 2 g을 정밀하게 달아 물 약 100 mL를 넣어 녹인다. 여기에 활성탄 10 g을 넣어 2 ∼ 3 분정도 끓인다. 식힌 다음 질산 (38 → 100) 1 mL를 넣어 진탕 혼화한 다음 물을 넣어 200 mL로 한 다음 여과한다. 여액 50 mL를 250 mL 플라스크에 정확하게 취하여 희석한 질산 (38 → 100) 2 mL 및 0.1 mol/L 질산은액 10 mL를 정확하게 넣은 다음 니트로벤젠 5 mL를 넣고 염화은이 석출될 때까지 진탕하여 혼화한다. 여기에 황산암모늄철시액 1 mL 넣고 과량의 질산은을 0.1 mol/L 티오시안산암모늄액으로 적정한다. 같은 방법으로 공시험을 한다. 다음 식으로 염화물의 양을 구한다. 검체에 염화물의 양이 많을 때에는 0.1 mol/L 질산은액을 증량한다.
A : 0.1 mol/L 티오시안산암모늄액의 소비량(mL)
A0 : 공시험 시 0.1 mol/L 티오시안산암모늄액의 소비량(mL)
B : 검액조제에 사용한 활성탄의 부피(mL)
나. 비타르색소
염화물시험법은 검체중에 불순물로서 들어있는 염화물의 허용한도량을 시험하는 방법이다. 그 한도는 염화물(Cl로서)의 중량백분율(%)로 나타낸다.
조 작 법 따로 규정이 없는 한 원료각조에서 규정하는 검체의 양을 네슬러관에 넣고 물 30㎖를 넣어 녹이고 묽은질산 6㎖ 및 물을 넣어 50㎖로 하여 검액으로 한다. 따로 원료각조에서 규정하는 양의 0.01N 염산을 넣고 묽은질산 6㎖ 및 물을 넣어 50㎖로 하여 비교액으로 한다. 이 때 검액이 맑지 않을 때에는 양쪽 액을 같은 방법으로 여과한다. 양쪽 액에 질산은 시액 1㎖씩을 넣어 잘 흔들어 섞고 차광된 곳에서 5분간 방치한 다음 흑색의 배경을 써서 네슬러관을 위 또는 옆에서 관찰할 때 검액의 혼탁도는 비교액보다 진하지 않다.
주 의 : 이 시험 또는 검액의 조제에 쓰이는 시약 및 시액은 공시험에서 혼탁하지 않거나 또는 거의 혼탁하지 않은 것을 쓴다.
21. 원자흡광광도법
원자흡광광도법은 빛이 원자증기층을 통과할 때 기저상태의 원자가 특유 파장의 빛을 흡수하는 현상을 이용하여 검체 중 피검원소의 양(농도)을 측정하는 방법이다.
장 치 보통 광원부, 검체원자화부, 분광부, 측광부 및 표시기록부로 되어 있다. 또 바탕보정부를 갖춘 것도 있다. 광원부에는 중공음극램프, 방전램프 등을 쓴다. 검체원자화부에는 화염방식, 전기가열방식 또는 냉증기방식을 쓰며, 냉증기방식에는 환원기화법 및 가열기화법이 있다. 화염방식은 버너 및 기체유량조절기, 전기가열방식은 전기가열로 및 전원부, 냉증기방식은 환원기화기, 가열기화기 등의 수은발생부 및 흡수셀로 되어 있다. 분광부에는 회절격자 또는 간섭필터를 쓴다. 측광부는 검출기 및 신호처리계 등으로 되어 있다. 표시기록부에는 표시화면, 기록장치 등이 있다. 바탕보정부는 바탕선을 보정하기 위한 것으로 연속스펙트럼광원방식, 지만 (Zeeman)방식, 비공명근접선방식, 자기방전방식 등이 있다. 특수장치로 셀렌 등을 분석할 때 쓰는 수소화물발생장치 및 가열흡수셀이 있다. 수소화물발생장치에는 저류식과 연속식이 있고, 가열흡수셀은 화염 또는 전기로에 의한 가열용이 있다.
조 작 법 따로 규정이 없는 한 다음 방법 중 하나에 따른다.
1) 화염방식 규정하는 광원램프를 끼우고 측광부에 전기를 넣어 광원램프를 켜고 분광기를 따로 규정하는 분석선파장에 맞춘 다음 적당한 전류값과 슬릿 폭을 설정한다. 규정하는 지연성 (支燃性)기체 및 가연성기체를 써서 이들 혼합기체에 점화하고 기체유량과 압력을 조절한 다음 용매를 화염 중에 분무하여 영점을 맞춘다. 규정하는 방법으로 만든 검액을 화염 중에 분무하여 그 흡광도를 측정한다.
2) 전기가열방식 규정하는 광원램프를 끼우고 측광부에 전기를 넣는다. 광원램프를 켜고 분광기를 따로 규정하는 분석선파장에 맞춘 다음 적당한 전류값과 슬릿 폭을 설정한다. 규정하는 방법으로 만든 검액의 일정량을 전기가열로 (발열체)에 주입하고 적당한 유량의 기체를 흘려 온도, 시간, 가열방식을 적당하게 설정하고 건조, 회화, 원자화하여 흡광도를 측정한다.
3) 냉증기방식 저압수은램프를 끼우고 측광부에 전기를 넣어 광원램프를 켜고 분광기를 따로 규정하는 분석선파장에 맞춘 다음 적당한 전류값와 슬릿 폭을 설정한다. 다음에 환원기화법에서는 규정하는 방법으로 만든 검액을 밀폐기에 취하고 적당한 환원제를 넣어 원소가 될 때까지 환원하여 기화시킨다. 또 가열기화법에서는 검체를 가열하여 기화시킨다. 이와 같은 방법으로 생긴 원자증기의 흡광도를 측정한다.
전처리법
1) 검체 약 1 g을 킬달플라스크에 정밀하게 달아 황산 6 mL 및 질산 10 mL를 넣어 천천히 가열한다. 액의 색이 어둡게 변하기 시작할 때 질산 10 mL를 넣고, 흰색의 연기가 발생할 때까지 가열한다. 이때 액의 색이 황색으로 되지 않을 경우에는 실온으로 식히고 질산 10 mL를 넣고 흰색연기가 발생할 때까지 가열하는 조작을 반복한다. 액의 색이 황색이 된 다음 실온으로 식히고 질산 5 mL 및 과염소산 3 mL를 넣어 액이 무색 및 담황색이 될 때까지 가열한다. 이것을 실온으로 식히고 포화수산ㆍ암모늄수화물용액 15 mL를 넣은 다음 아황산가스의 흰 연기가 날 때 까지 가열한다. 다시 실온으로 식히고 물 20 mL를 넣고 끓을 때까지 가열한 후 실온까지 식히고 물을 넣어 정확하게 50 mL로 한다.
2) 검체 약 1 g을 킬달플라스크에 정밀하게 달아 질산 5 mL를 넣어 천천히 가열한 후 질산ㆍ과염소산혼합액(1 : 1) 3 mL를 넣고 건고되지 않도록 주의하여 천천히 가열한다. 이 경우에 있어서 건고되면 폭발할 우려가 있으므로 가열의 조작은 충분히 주의하여야 한다. 이것을 실온에서 냉각한 후 질산 ㆍ과염소산혼합액(1 : 1) 3 mL를 추가로 넣어 건고되지 않도록 주의하면서 천천히 가열하여 농축한다. 실온이 될 때까지 냉각한 후 물 20 mL 및 묽은염산(1 → 10) 20 mL를 넣어 10분간 끓인 후 여지를 이용하여 여과하고 이 액에 물을 넣어 50 mL로 한다.
3) 검체 약 1 g을 킬달플라스크에 정밀하게 달아 질산 5 mL를 넣어 천천히 가열한 후 질산ㆍ과염소산혼합액(1 : 1) 3 mL를 넣어 건고되지 않도록 주의하면서 천천히 가열 농축한다. 건고되면 폭발할 우려가 있으므로 가열의 조작은 충분히 주의하여야 한다. 이 경우에 있어서 액의 색이 완전히 무색투명하게 된 후 실온으로 식히고 질산ㆍ과염소산혼합액(1 : 1) 3 mL를 넣어 건고되지 않도록 주의하면서 천천히 가열하여 농축한 조작을 3회 반복한다. 여기에 실온으로 식히고 물을 넣어 50 mL로 한다.
검액조제법
1) 전처리법 1) 또는 2)에서 얻은 용액의 10 mL를 100 mL 분액여두에 정확하게 달아 브롬티몰블루시액 2 방울을 지시약에 넣어 묽은암모니아수(28)(1 → 2)를 넣어 중화시킨 후 아세트산ㆍ아세트산나트륨완충액 10 mL를 넣어 pH 값이 6이 될 때까지 조절한다. 여기에 주석산나트륨칼륨완충액(1 → 4) 5 mL를 넣어 포화황산암모늄용액 10 mL 및 N,N-디에틸디티오카르바민산나트륨삼수화물용액(1 → 50) 10 mL를 넣은 후 4-메틸-2-펜타논 10 mL를 정확하게 넣어 5 분간 세게 흔들어 섞고 4-메틸-2-펜타논층을 검액으로 한다.
2) 전처리법 3)에서 얻은 용액 25 mL를 정확하게 취하여 브롬티몰블루시액 2 방울을 지시약에 넣어 묽은암모니아수(28)(1 → 2)를 넣어 중화시킨 후 물을 넣어 50 mL로 하고 100 mL의 분액여두로 옮긴다. 여기에 아세트산ㆍ아세트산나트륨완충액 10 mL 및 N,N-디에틸디티오카르바민산나트륨삼수화물용액(1 → 50) 10 mL를 넣은 후 4-메틸-2-펜타논 10 mL를 정확하게 넣어 5분간 세게 흔들어 섞고 4-메틸-2-펜타논층을 검액으로 한다.
3) 전처리법 3)에서 얻은 용액 25 mL를 정확하게 취하여 묽은황산(3 → 50) 10 mL를 넣고 물을 넣어 50 mL로 한 다음 과망간산칼륨시액 2방울 내지 3방울을 넣어 가열한다. 이 경우에 액의 자홍색이 없어질 때까지 과망간산칼륨시액을 넣는 조작을 반복한다. 액의 보라색이 없어지지 않으면 브롬티몰블루시액 2방울을 지시약에 넣어 묽은암모니아수(28)(1 → 2)를 넣어 중화시킨 후 100 mL의 분액깔대기로 옮긴다. 여기에 아세트산ㆍ아세트산나트륨완충액 10 mL 및 N,N-디에틸디티오카르바민산나트륨삼수화물용액(1 → 50) 10 mL를 넣은 후 4-메틸-펜타논 10 mL를 정확하게 넣어 5 분간 세게 흔들어 섞고 4-메틸-2-펜타논층을 검액으로 한다.
4) 전처리법 2)에서 얻은 용액 10 mL를 100 mL의 분액여두에 정확하게 달아 암모니아수(28)를 넣어 pH가 8.5가 되도록 조정한다. 여기에 시안화칼륨용액(1→20) 4 mL 및 N,N-디에틸디티오카르바민산나트륨삼수화물용액(1 → 50) 10 mL를 넣은 후 4-메틸-2-펜타논 10 mL를 정확하게 넣어 5분간 세게 흔들어 섞고 4-메틸-2-펜타논층을 검액으로 한다.
5) 따로 규정이 없는 한, 전처리하지 않은 검체 5∼10g을 정밀히 달아 도가니 또는 백금접시에 넣어 건조하고 탄화시킨 다음 450∼550℃에서 회화한다. 회화가 잘 되지 않으면 일단 식힌 다음 이에 회화보조제로서 희석시킨 질산(1→2) 또는 50% 질산마그네슘용액 또는 질산알루미늄ㆍ질산칼슘용액(질산알루미늄 40g 및 질산칼슘 20g을 물 100mL에 녹인 액)을 2∼5mL 가하여 적신 다음 건조하고 회화를 계속한다. 회화가 충분하지 않을 때에는 위의 조작을 1회 반복하고 필요하면 마지막으로 질산(1→2) 2∼5mL를 가하여 회화한다. 회화가 끝나면 잔류물을 물로 적셔주고 염산 2∼4mL를 가하여 증발건고시킨 다음 각 시험법에서 정한 용매(주석은 1N 염산, 그 밖의 금속은 0.5N 질산)를 가해주고 가온하여 녹인 다음 불용물이 있으면 여과지로 여과하고 따로 규정이 없는 한, 0.5N 질산을 가하여 25mL로 한 액을 검액으로 한다. 다만, 회화보조제인 질산염 또는 질산은 시험조작에 영향이 없을 때에만 사용한다. 공시험용액에 대해서도 같은 조작을 하여 검액을 보정한다.
정 량 법 보통 다음 방법 중 하나에 따른다. 특히 정량할 때에는 간섭 및 바탕선을 고려할 필요가 있다.
1) 검량선법 농도가 다른 3 가지 이상의 표준액을 만들어 각 표준액의 흡광도를 측정하여 얻은 값으로부터 검량선을 작성한다. 다음 측정 가능한 농도범위에 들도록 만든 검액의 흡광도를 측정한 다음 검량선에서 피검원소의 양(농도)을 구한다.
2) 표준첨가법 같은 양의 검액 3 개 이상을 취하여 각각에 피검원소가 단계적 농도가 되도록 피검원소표준액를 첨가하고 다시 용매를 넣어 일정 용량으로 한다. 각 용액을 가지고 흡광도를 측정하여 첨가한 표준피검원소의 양을 가로축으로 하고 흡광도를 세로축으로 하여 검량선을 작성한다. 여기에서 얻은 회귀선을 연장하여 가로축과 만나는 점과 원점과의 거리에서 피검원소의 양(농도)을 구한다. 다만 이 방법은 1)에 의한 검량선이 원점을 지나는 직선일 경우에만 적용된다.
3) 내부표준법 내부표준원소의 양을 일정하게 하고 표준피검원소의 기지량을 각각 단계적 농도가 되도록 첨가하여 표준액을 만든다. 각 표준액을 가지고 각 원소의 분석선파장에서 표준피검원소에 의한 흡광도 및 내부표준원소에 의한 흡광도를 같은 조건으로 측정하여 표준피검원소에 의한 흡광도와 내부표준원소에 의한 흡광도와의 비를 구한다. 표준피검원소의 양(농도)을 가로축으로 하고 흡광도비를 세로축으로 하여 검량선을 작성한다. 검액을 만들 때에는 미리 표준액의 경우와 같은 양의 내부표준원소를 넣는다. 다음에 검량선을 작성할 때와 같은 조건으로 얻은 피검원소에 의한 흡광도와 내부표준원소에 의한 흡광도와의 비를 구하여 검량선에서 피검원소의 양(농도)을 구한다.
주의 : 시약·시액 및 기체는 측정을 방해하지 않는 것을 쓴다.
22. 유도결합플라즈마발광광도법
가. 장 치
일반적으로 여기원부, 시료도입부, 발광부, 분광부, 측광부 및 표시기록부로 되어 있다. 여기원부는 시료를 여기시키고, 발광시켜 전기에너지를 공급하고 제어하는 전원, 제어계 및 회로로 되어있고, 부속으로 가스공급원과 냉각장치를 포함한다. 시료도입부는 네블라이져와 분무기로 되어있다. 발광부는 토치관과 고주파유도코일등으로 되어 있다. 분광부는 집광계, 회절격자등의 분광기로 되어 있다. 측광부는 검출기와 신호처리계로 되어 있다. 표시기록부에는 디스플레이, 기록장치 등이 있다. 방식으로는 파장주사형 분광기를 이용하는 단원소 축차분석방식, 파장주사형 분광기를 이용하는 다원소 축차분석방식 및 파장고정형의 폴리크로메터를 이용하는 다원소 동시분석방식이 있다.
나. 시험용액의 조제
따로 규정이 없는 한, 원자흡광광도법의 나. 시험용액의 조제에 따른다.
다. 조작법
일반적으로 전류가 통하는 부분에 이상이 없는 것을 확인한 후, 여기원부 및 제어장치의 전원 스위치를 켠다. 진공형분광기를 이용하는 진공자외선 영역의 발광선을 측정하는 경우에는 발광부와 분광기 간의 광축을 알곤 또는 질소로 10분간 치환한다. 알곤 또는 질소를 일정량의 유량으로 설정하고, 고주파 전원을 켜고 플라즈마를 점화한다. 수은램프의 발광선을 이용하여 분광기의 파장을 교정한다. 따로, 규정한 방법으로 조제한 시험용액 및 표준용액의 일정량을 도입하고 적당한 발광 스펙트럼선의 발광강도를 측정한다.
라. 정량법
보통 다음의 어느 한 방법에 따른다. 특히 정량을 할 때는 간섭(干涉) 및 공시험보정(Back ground)을 고려할 필요가 있다.
(1) 검량선법 : 3종 이상의 농도가 다른 표준용액을 조제하고 각각의 표준용액에 대한 그 발광강도를 측정하여 얻은 값으로부터 검량선을 작성한다. 다음 측정가능한 농도범위로 조제한 시험용액의 흡광도를 측정한 다음 검량선으로 부터 목적원소량(농도)을 구한다.
(2) 표준첨가법 : 같은 양의 시험용액 3개 이상을 취하여 각각에 목적원소가 단계적으로 함유되도록 표준용액을 첨가하고 이에 용매를 넣어 일정용량으로 한다. 각 용액의 발광강도를 측정하고 횡축에 첨가한 표준목적원소량(농도), 종축은 발광강도로 하여 그래프에 각각의 값을 그려 넣는다. 이 그려 넣은 값으로 얻어진 회귀선을 연장하여 횡축과 만나는 점과 원점과의 거리로써 목적원소량(농도)을 구한다. 다만, 이 방법은 (1)에 의한 검량선이 원점을 지나는 직선일 경우에만 적용된다.
(3) 내부표준법 : 내부표준원소의 일정량에 대하여 표준목적원소의 기지량을 각각 단계적으로 함유되도록 표준용액을 첨가하고 이에 용매를 넣어 일정용량으로 한다. 각각의 용액을 취해 각 원소의 분석선파장에서 표준대상원소에 의한 발광강도 및 내부표준원소의 의한 발광강도를 동일조건에서 측정하고 표준대상원소에 의한 발광강도와 내부표준원소에 의한 발광강도의 비를 구한다. 횡축에 첨가한 표준목적원소량(농도), 종축은 발광강도의 비로 하여 검량선을 작성한다. 다음 시험용액의 조제는 표준용액의 경우와 같이 동량의 내부표준원소를 넣는다. 다음에 검량선을 작성할 때와 같은 조건으로 얻은 목적원소에 의한 발광강도와 내부표준원소에 의한 발광강도와의 비를 구하여 검량선으로부터 목적원소량(농도)을 구한다.
(※ 주의 : 시험에 쓰는 시약, 시액은 측정에 방해가 되지 않는 것을 쓴다.)
23. 융점측정법
융점은 보통 결정성물질이 가열로 융해하여 고상과 액상이 평형상태가 될 때의 온도로 정의하지만 실용적으로는 검체를 가열 승온하는 과정에서의 상태변화를 관찰하여 융해종점의 온도를 측정하여 융점으로 한다. 융점은 순수물질에서는 각각의 물질의 고유한 값을 나타내므로 물질의 동정, 확인 및 순도의 지표로 쓴다.
융점은 다음 중 한 방법으로 측정한다. 비교적 순도가 높고 가루로 만들 수 있는 물질은 제 1 법으로, 물에 불용성이고 가루로 하기 어려운 물질은 제 2 법으로, 바셀린 류의 융점은 제 3 법으로 측정한다.
측정은 따로 규정이 없는 한 제 1 법으로 측정한다.
제 1 법 보통 비교적 순도가 높고 가루로 만들기 쉬운 것은 이 방법으로 측정한다.
1) 장 치 그림과 같은 장치를 쓴다.
다만 교반, 가온 및 냉각조작 등이 자동화 된 장치도 쓸 수 있다.
욕액 상온에서 동점도 50 ∼ 100 mm2/s의 맑은 실리콘유를 쓴다.
침선부온도계 측정온도범위에 따라 1호 ∼ 6호의 온도계가 있다. 융점이 50 ℃ 미만일 때는 1 호, 40 ℃ 이상 100 ℃ 미만일 때는 2 호, 90 ℃ 이상 150 ℃ 미만일 때는 3 호, 140 ℃ 이상 200 ℃ 미만일 때는 4 호, 190 ℃ 이상 250 ℃ 미만일 때는 5 호, 240 ℃ 이상 320 ℃ 미만일 때는 6 호를 쓴다.
모세관 안지름 0.8 ∼ 1.2 mm, 길이 120 mm, 벽의 두께 0.2 ∼ 0.3 mm이며 한쪽 끝이 막힌 경질유리로 만든 것을 쓴다.
2) 조작법 검체를 고운 가루로 하여 따로 규정이 없는 한 데시케이터 (실리카겔)에서 24 시간 건조한다. 또 건조 후라고 할 때에는 건조감량 항의 조건으로 건조한 것을 쓴다. 이 검체를 건조한 모세관 H에 넣고 막힌 끝 쪽을 밑으로 하여 유리판 또는 자기판 위에 세운 길이 약 70 cm의 유리관 안에 떨어뜨려 튀게 하여 단단하게 채워서 층의 두께가 3 mm 또는 이에 가까운 두께가 되도록 한다. 욕액 B를 가열하여 예상한 융점보다 약 10 ℃ 낮은 온도까지 천천히 올려 침선부온도계 D의 침선을 욕액의 메니스커스에 일치시키고 검체를 넣은 모세관 H를 코일용수철 G에 끼워 검체를 넣은 부분이 온도계 D의 수은구 가운데에 오도록 한다. 1 분간에 약 3 ℃ 올라가도록 가열하다가 예상한 융점보다 약 5 ℃ 낮은 온도부터는 1 분간에 1 ℃ 올라가도록 가열한다. 검체가 모세관 H 안에서 액화하여 고체를 전혀 볼 수 없게 되었을 때 온도계 D의 눈금을 읽어 융점으로 한다.
장치의 적합성 장치의 적합성의 확인은 융점표준품을 써서 정기적으로 한다. 융점표준품은 2호 ∼ 5호 온도계를 쓰는 경우의 장치적합성평가를 위하여 조제된 것으로 다른 융점을 가지는 6 종류의 고순도 물질 (아세트아닐리드, 아세토페네티딘, 카페인, 설파닐아미드, 설파피리딘, 바닐린)이 선택되어 있고 각 물질의 융점 MPf (융해종점의 온도)이 표시되어 있다. 예상되는 검체의 융점에 맞는 온도계 및 융점표준품을 선택하여 조작법에 따라 융점표준품의 융점을 측정할 때 바닐린 및 아세트아닐리드의 융점은 MPf ± 0.5 ℃, 아세토페네티딘 및 설파닐아미드의 융점은 MPf ± 0.8℃, 설파피리딘 및 카페인의 융점은 MPf ± 1.0℃ 의 범위에 있을 때 장치의 적합성이 확인된 것으로 한다. 다만 위의 측정은 3 회 반복하여 그 평균값을 융점으로 한다. 그러나 부적합으로 판정된 때는 위의 조작법에 따라 검체의 충전, 온도계 및 모세관의 위치, 욕액의 가열·교반, 온도상승속도의 제어 등이 올바른 지를 확인하여 재시험을 한다. 이들 조건 설정이 올바fms 데도 위의 판정기준에 적합하지 않을 때는 침선부온도계를 재검정하거나 교환할 필요가 있다.
제 2 법 지방, 지방산, 파라핀 또는 납(蠟) 등에 적용한다.
1) 장치 제 1 법의 장치와 달리 물을 넣은 비커를 욕액 및 가열용기로 쓴다. 온도계는 침선부온도계 또는 전몰식온도계를 쓴다. 또한 모세관은 제 1 법에 규정된 것과 같은 것으로 양 끝이 열려있는 것을 쓴다.
2) 조작법 검체를 조심하면서 될 수 있는 대로 낮은 온도에서 융해하고 거품이 들어가지 않도록 조심하면서 모세관 속에 빨아 올려 약 10 mm의 높이가 되도록 한다. 모세관으로부터 검체가 흘러나오지 않도록 하여 10 ℃ 이하에서 24 시간 방치하거나 적어도 1 시간 얼음 위에 방치한 다음 검체의 위치가 수은구의 가운데 바깥쪽에 오도록 고무줄로 온도계에 붙들어 맨다. 모세관을 단 온도계를 물을 넣은 비커에 넣어 검체의 아래 끝을 수면 아래 30 mm의 위치에 고정한다. 물을 계속 저어주면서 가온하여 예상한 융점보다 5 ℃ 낮은 온도에 이르렀을 때부터 1 분간에 1 ℃ 올라가도록 가열한다. 모세관에서 검체가 떠오를 때의 온도계의 온도를 읽어 융점으로 한다.
제 3 법 바셀린류에 적용한다.
1) 장치 제 1 법의 장치와 달리 물을 넣은 비커를 욕액 및 가열용기로 쓴다. 온도계는 침선부온도계 또는 전몰식온도계를 쓴다.
2) 조작법 검체를 잘 저어 섞으면서 천천히 90 ∼ 92 ℃까지 가열하여 융해한 다음 가열을 그치고 검체를 융점보다 8 ∼ 10 ℃ 높은 온도까지 방치하여 식힌다. 온도계 (침선부 또는 전몰식)를 5 ℃로 식혀 닦아서 건조하고 곧 수은구의 반정도를 검체에 삽입하였다가 바로 빼내어 수직으로 하고 방치하여 식혀 묻은 검체가 혼탁하여질 때 16 ℃ 이하의 물속에 5 분간 담가 둔다. 다음에 시험관에 온도계를 넣어 온도계의 아래 끝과 시험관의 바닥 사이가 15 mm가 되도록 코르크마개로 온도계를 고정한다. 이 시험관을 약 16 ℃의 물이 들어 있는 비커 속에 매달고 수욕의 온도가 30 ℃가 될 때까지는 1 분간에 2 ℃ 올라가도록하고 그 다음부터는 1 분간에 1 ℃ 올라가도록 가열한다. 온도계로부터 최초의 1 방울이 떨어질 때의 온도를 측정한다. 이 조작을 3 회 반복하여 측정값의 차가 1 ℃ 미만일 때에는 그 평균값을, 1 ℃ 이상일 때는 다시 이 조작을 2 회 반복하여 모두 합한 5 회의 평균값을 융점으로 한다.
24. 자외가시부흡광도측정법
자외가시부흡광도측정법은 검체를 각조에서 규정하는 용매에 녹여 흡수 극대파장을 측정하여 그것에 따라 확인시험을 한다. 흡수의 극대파장에 있어 일정농도의 용액의 흡광도를 측정하여 정량을 할 수도 있다.
장 치 분광광도계를 이용한다. 가시부를 측정할 때는 광원에 있어 텅스텐램프 또는 할로겐 램프를 이용한다. 가시부의 흡수측정에는 유리제 또는 석영제의 층장 1 cm의 셀을 이용한다.
조 작 법 규격에 있어 규정하는 용액을 가지고 시험을 한다. 확인시험은 흡광도가 0.2에서 0.7까지의 범위가 되지 않는 경우에는 0.2에서 0.7의 범위가 되도록 규격에 정해져 있는 용매로 조정한다. 정량은 규격에 정해져 있는 흡수극대파장에서 흡광도(A)를 측정하고 다음에 식에 따라 정량한다.
B:각각의 검체의 규격에 있어 규정하는 흡광계수. 이 경우에 있어 흡광계수는 색소 1 mg을 용매 1 L에 녹이고 층장 1 cm의 셀을 이용하여 측정한 흡광도를 말한다.
N:검액 중의 검체 농도(ppm)
파장 및 흡광도의 교정 파장교정용광학필터를 써서 각각의 필터에 첨부된 시험성적서의 시험조건으로 시험성적서에 표시된 기준값의 파장부근에서의 투과율을 측정하고 투과율이 극소값을 나타내는 파장을 읽는 시험을 할 때 그 측정파장과 기준값 파장과의 편차는 ± 0.5 nm 이내이고, 측정을 3회 반복할 때 측정값은 모두 평균값 ± 0.2 nm 이내이다. 또 파장은 저압수은램프의 253.65 nm,365.02 nm,435.84 nm 또는 546.07 nm 또는 중수소 방전관의 486.00 nm 또는 656.10 nm의 휘선을 써서 시험할 수 있다. 이때의 측정파장과 휘선의 파장과의 편차는 ± 0.3 nm 이내이고 측정을 3회 반복할 때 측정값은 모두 평균값 ± 0.2 nm 이내이다.
투과율 또는 흡광도는 투과율교정용 광학필터를 써서 각각의 필터에 첨부된 시험성적서의 시험조건으로 시험성적서에 표시된 기준값의 파장에서의 투과율을 읽는 시험을 할 때 그 측정투과율과 기준투과율과의 편차는 시험성적서에 표시된 상대정밀도의 상한값 및 하한값에 각각 1 %를 더한 값 이내이고 측정을 3회 반복할 때 흡광도의 측정값 (또는 투과율의 측정값을 흡광도로 환산한 값)은 흡광도가 0.500 이하일 때 모두 평균값 ± 0.002 이내이고, 흡광도가 0.500를 넘을 때는 모두 평균값 ± 0.004이내이다. 또한 동일파장에서 투과율이 다른 여러 장의 투과율교정용 광학필터를 써서 투과율의 직선성을 확인하는 것이 바람직하다.
파장 및 투과율교정용광학필터
필터의 종류 | 파장교정범위(nm) | 품명 |
파장교정용 네오디뮴광학필터 | 400∼750 | KCRM001 |
파장교정용 홀뮴광학필터 | 250∼600 | KCRM002 |
투과율교정용광학필터는 다음 표시된 것을 이용한다.
25. 적외부스펙트럼측정법
적외부스펙트럼측정법은 물질의 적외부스펙트럼이 그 물질의 화학구조에 따라 정해지는 성질을 이용하여 여러 종류의 파수에 있어 흡수 또는 투과되는 스펙트럼을 측정함에 따라 물질을 확인하는 방법이다.
장치 및 조정법 분산형적외분광광도계 또는 푸리어변환형적외분광광도계 (Fourier transform infrared spectrophotometer)를 쓴다.
1) 투과율 (%)의 차 미리 분산형적외분광광도계 또는 푸리어변환형적외분광광도계를 가지고 두께 0.04 mm의 폴리스티렌막의 흡수스펙트럼을 측정하여 얻어진 흡수스펙트럼의 2870 cm-1 부근의 극소와 2851 cm-1 부근의 극대투과율 (%)의 차이가 18 % 이상이다. 또한 1589 cm-1 부근의 극소와 1583 cm-1 부근의 극대투과율 (%)의 차이는 12 % 이상인 것을 확인한다.
2) 파수의 눈금 파수의 눈금은 보통 폴리스티렌막의 아래의 흡수대 중에서 몇 개를 써서 보정한다. 다만 괄호안의 값은 이 값의 정확성을 나타낸다.
3027.1 (± 0.3) | 1871.0 (± 0.3) | 1181.4 (± 0.3) |
1028.0 (± 0.3) | 2924 (± 2) | 1801.6 (± 0.3) |
1154.3 (± 0.3) | 906.7 (± 0.3) | 2850.7 (± 0.3) |
1601.4 (± 0.3) | 1069.1 (± 0.3) | 698.9 (± 0.5) |
1944 (± 1) | 1583.1 (± 0.3) | |
3) 투과율 및 파수의 재현성 투과율 및 파수의 재현성은 폴리스티렌막의 3000 ∼ 1000 cm-1에서의 몇 점의 투과율을 2 회 반복 측정할 때 투과율의 차이는 0.5 % 이내, 파수의 차이는 3000 cm-1 부근에서 5cm-1, 1000 cm-1 부근에서 1 cm-1 이내로 한다.
검체의 조제 및 측정 고체검체 1 ∼ 2 mg을 마노약절구에 넣고 가루로 하여 브롬화칼륨 (적외부스펙트럼측정용) 100 mg ∼ 200mg을 넣어 습기를 흡수하지 않도록 조심하면서 빨리 잘 갈아 섞은 다음 정제성형기로 압축하여 정제로 만든다. 다만 투명한 정제를 만들 때는 0.67 kPa 이하로 감압하고 정제의 단위면적 (cm2)당 5 ∼ 10 t의 압력을 5 ∼ 8 분간 가하여 정제로 만든다. 검체는 주된 흡수대의 투과율이 5 ∼ 80 %가 되도록 조제한다.
확인방법 확인하고자 하는 물질의 특성 흡수파수가 의약품각조에서 규정하는 흡수파수와 일치하는가를 확인하여 검체가 의약품각조 의약품과 같은 물질임을 확인한다.
26. 정 량 법
정량법은 제 1 법,제 2 법 또는 제 3 법에 의하여 색소 함량을 정량한 방법이다.
조 작 법 제 1 법 검체 약 0.5 g를 정밀하게 달아 물 50 mL를 넣어 녹이고 이것을 500 mL의 비커에 옮기고 끓을 때까지 가열한 후 묽은염산(1 → 50) 25 mL를 넣어 다시 가열한다. 다음에 비커의 내벽을 소량의 물로 씻은 다음 비커의 입구를 시계접시로 덮고 끓는 물에서 약 5 시간 가열한다. 실온으로 식히고 침전물을 질량을 이미 알고 있는 유리여과기(1G4)로 여과하고 묽은염산(1 → 200) 10 mL 씩 3회, 물로 약 10 mL씩 2회 씻는다. 침전물을 도가니 형태 유리 여과기에 넣고 105 ℃로 3 시간 건조하고, 데시케이터(실리카겔)에서 식힌 후 그 질량을 정밀하게 달고 다음의 식에 따라 색소의 함량을 구한다.
k:규격에 있어 규정한 계수
제 2 법 검체 약 0.5 g를 정밀하게 달고 묽은수산화나트륨시액 50 mL를 넣어 녹이고 이것을 500 mL의 비커에 옮기고 끓을 때까지 가열한 다음 묽은염산(1 → 50) 25 mL를 넣고 다시 가열한다. 다음에 비커의 내벽을 소량의 물로 씻은 다음 비커의 입구를 시계접시로 덮고 끓는 물에서 약 5 시간 가열한다. 실온으로 식히고 침전물을 질량을 이미 알고 있는 유리여과기(1G4)로 여과하고 묽은염산(1 → 200) 10 mL 씩 3회, 물로 약 10 mL씩 2회 씻는다. 침전물을 도가니 형태 유리 여과기에 넣고 105 ℃로 3 시간 건조하고, 데시케이터(실리카겔)에서 식힌 후 그 질량을 정밀하게 달고 제 1 법과 동일한 식에 따라 색소의 함량을 구한다.
제 3 법 검체 약 0.1 g를 50 mL 비커에 넣고 정밀하게 질량을 달고 황산 5 mL를 넣고 수욕에서 가온하여 녹인다. 실온으로 식히고 물 약 100 mL를 넣은 300 mL 용량의 삼각플라스크로 옮긴다. 비커 중에 잔류물은 물 약 20 mL를 넣어 삼각플라스크에 씻어 넣는다. 여기에 생긴 침전물을 질량을 이미 알고 있는 도자기형태 유리여과기(1G4)로 여과한다. 물 15 mL 씩 6회 씻는다. 침전물을 비커에 옮기고 끓을 때까지 가열한 다음 묽은 염산(1 → 50) 25 mL를 넣고 다시 가열한다. 다음에 비커의 내벽을 소량의 물로 씻은 다음 비커의 입구를 시계접시로 덮고 끓는 물에서 약 5시간 가열한다. 실온이 될 때가지 냉각한 후 침전물을 질량을 이미 알고 있는 유리여과기(1G4)로 여과하고 침전물을 도가니 형태 유리 여과기에 넣고 85 ℃에서 항량이 될 때까지 건조한 후 데시케이터(실리카겔)에서 식힌 다음 그 질량을 정밀하게 달고 제 1 법과 동일한 식에 따라 색소의 함량을 구한다.
27. 정성반응
정성반응은 원료각조의 확인시험에 적용하는 것으로 따로 규정이 없는 한 혼합물질에 대해서는 쓰지 않는다.
마그네슘염
1) 마그네슘염의 용액에 탄산암모늄시액을 넣을 때 백색의 침전이 생기고 염화암
모늄시액을 추가할 때 침전은 녹는다. 여기에 인산일수소나트륨시액을 추가할 때 백색의 결정성 침전이 생긴다.
2) 마그네슘염의 용액에 수산화나트륨시액을 넣을 때 백색의 겔상침전이 생기며 과량의 시액을 넣어도 침전은 녹지 않으나 요오드시액을 추가할 때 침전은 어두운 갈색으로 된다.
망 간 염
1) 망간염의 용액에 암모니아시액을 넣으면 흰색의 침전이 생긴다. 그 일부에 질산은시액을 추가하면 침전은 검정색으로 변한다. 또 다른 일부를 방치하면 침전의 상부가 갈색으로 된다.
2) 망간염의 묽은질산산성용액에 비스무트산나트륨의 가루 소량을 넣을 때 액은 자주색을 나타낸다.
바륨염
1) 바륨염을 염산으로 적시고 불꽃반응을 볼 때 지속하는 황록색을 나타낸다.
2) 바륨염의 용액에 묽은황산을 넣을 때 백색겔상침전이 생기고 묽은질산을 추가하여도 침전은 녹지 않는다.
비스머스염
1) 비스머스염에 될 수 있는 대로 소량의 염산을 넣어 녹이고 물을 넣어 희석할 때 백탁이 생긴다. 여기에 황산나트륨시액 1~2방울을 추가할 때 어두운 갈색의 침전이 생긴다.
2) 비스머스염의 염산산성용액에 치오뇨소시액티오우레아시액을 넣을 때 액은 황색을 나타낸다.
3) 비스머스염의 묽은질산 또는 묽은황산용액에 요오드화칼륨시액을 적가할 때 흑색의 침전이 생기고 요오드화칼륨시액을 추가할 때 침전은 녹고 등색을 나타낸다.
아연염
1) 아연염의 중성 또는 알칼리성용액에 아황산암모늄시액 또는 아황산나트륨시액을 넣을 때 백색의 침전이 생긴다. 침전을 분리하여 묽은아세트산을 넣어도 녹지 않지만 묽은염산을 추가할 때 녹는다.
2) 아연염의 용액에 페로시안화칼륨시액을 넣을 때 백색의 침전이 생기며 묽은염산을 추가하여도 침전은 녹지 않는다.
3) 아연염의 용액에 인산을 넣어 산성으로 하고 황산동용액(1→1000) 1방울 및 치오시안산수은암모늄시액티오시안산수은암모늄시액 2㎖를 넣을 때 엷은 자색의 침전이 생긴다.
알루미늄염
1) 알루미늄염의 용액에 염화암모늄시액 및 암모니아시액을 넣을 때 백색의 겔상 침전이 생기고 이 침전은 과량의 암모니아시액에 녹지 않는다.
2) 알루미늄염의 용액에 수산화나트륨시액을 넣을 때 백색의 겔상 침전이 생기며 과량의 수산화나트륨시액을 추가할 때 침전은 녹는다.
3) 알루미늄염의 용액에 황화나트륨시액을 넣을 때 백색의 겔상 침전이 생기며 과량의 황화나트륨시액을 추가할 때 침전은 녹는다.
4) 알루미늄염의 용액에 백색의 겔상 침전이 생길 때까지 암모니아시액을 넣고 알리자린에스시액알리자린레드 S 시액 5방울을 추가할 때 침전은 적색으로 변한다.
염화물
1) 염화물의 용액에 황산 및 과망간산칼륨을 넣어 가열할 때 염소의 냄새가 나며 이 가스는 물에 적신 요오드화칼륨‧전분지를 변화시킨다.
2) 염화물의 용액에 질산은 시액을 넣을 때 백색의 침전이 생긴다. 침전을 분리하여 그 일부에 묽은질산을 넣어도 녹지 않으며 다른 일부에 과량의 수산화암모늄시액을 넣을 때 녹는다.
철(Ⅱ)염
1) 철(Ⅱ)염의 약산성용액에 페리시안화칼륨시액을 넣을 때 청색의 침전이 생기며 묽은염산을 추가하여도 침전은 녹지 않는다.
2) 철(Ⅱ)염의 용액에 수산화나트륨시액을 넣을 때 회록색의 겔상 침전이 생기며 아황산나트륨시액을 추가할 때 흑색의 침전이 생기고 여기에 묽은염산을 넣을 때 녹는다.
철(Ⅲ)염
1) 철(Ⅲ)염의 약산성용액에 페로시안화칼륨시액헥사시아노철(II)산칼륨시액을 넣을 때 청색의 침전이 생기며 묽은염산을 추가하여도 침전은 녹지 않는다.
2) 철(Ⅲ)염의 용액에 수산화나트륨시액을 넣을 때 적갈색겔상 침전이 생기며 황화나트륨시액을 추가할 때 침전은 흑색으로 변한다. 침전을 분리하여 묽은염산을 넣을 때 침전은 녹고 액은 백탁한다.
3) 철(Ⅲ)염의 약산성용액에 설포살리실산시액을 넣을 때 액은 자색을 나타낸다.
칼륨염
1) 칼륨염을 염산에 적시고 불꽃반응을 보면 엷은 자색을 나타낸다. 불꽃이 황색이면 코발트유리를 통하여 관찰할 때 적자색으로 보인다.
2) 칼륨염의 중성용액(1→20)에 주석산수소나트륨시액타르타르산수소나트륨시액을 넣을 때 백색의 결정성 침전이 생긴다. 침전의 생성을 빠르게 하려면 유리막대로 시험관의 안벽을 긁어준다. 이 침전을 분리하여 암모니아시액, 수산화나트륨시액 또는
탄산나트륨시액을 넣을 때 다 녹는다.
3) 칼륨염의 아세트산산성용액(1→20)에 아질산코발트나트륨시액헥사니트로코발트(III)산나트륨시액을 넣을 때 황색의 침전이 생긴다.
4) 칼륨염에 과량의 수산화나트륨시액을 넣어 가온하여도 암모니아 냄새가 나지 않는다(암모늄염과의 구별).
칼슘염
1) 칼슘염을 염산에 적시고 불꽃반응을 보면 적색을 나타낸다.
2) 칼슘염의 용액에 탄산암모늄시액을 넣을 때 백색의 침전이 생긴다.
3) 칼슘염의 용액에 수산암모늄시액을 넣을 때 백색의 침전이 생긴다. 침전을 분리하여 그 일부에 묽은아세트산을 넣어도 녹지 않는다. 또한 다른 일부에 묽은염산을 넣을 때 녹는다.
4) 칼슘염의 중성용액에 크롬산칼륨시액 10방울을 넣어 가열하여도 침전이 생기지 않는다(스트론튬염과의 구별).
탄산염
1) 탄산염에 묽은염산을 넣을 때 거품을 내면서 가스가 나온다. 이 가스를 수산화칼슘시액중에 통할 때 곧 백색의 침전이 생긴다(탄산수소염과 공통).
2) 탄산염용액에 황산마그네슘시액을 넣을 때 백색의 침전이 생기고 묽은아세트산을 추가할 때 침전은 녹는다.
3) 탄산염의 냉용액에 페놀프탈레인시액 1방울을 넣을 때 액은 홍색을 나타낸다(탄산수소염과 구별).
황산염
1) 황산염의 용액에 염화바륨시액을 넣을 때 백색의 침전이 생기며 묽은질산을 추가하여도 침전은 녹지 않는다.
2) 황산염의 중성용액에 아세트산납시액아세트산납시액을 넣을 때 백색의 침전이 생기며 아세트산암모늄시액아세트산암모늄시액을 추가할 때 녹는다.
3) 황산염의 용액에 같은 용량의 묽은염산을 넣어도 백탁이 생기지 않는다(치오티오황산염과의 구별). 또한 이산화황의 냄새가 나지 않는다(아황산염과의 구별).
28. 중금속시험법
중금속이란 산성에서 황화나트륨시액에 의하여 색을 나타내는 금속성혼재물을 말하며 그 양은 납 (Pb)의 양으로 나타낸다. 의약품각조에는 중금속 (Pb로서)의 한도를 ppm으로 ( )안에 나타낸다.
검액 및 비교액의 조제법 검체 약 1.0 g 을 달아 석영 또는 사기도가니에 넣고 느슨하게 뚜껑을 덮고 약하게 가열하여 탄화한다. 식힌 다음 질산 2 mL 및 황산 5 방울을 넣고 흰 연기가 나지 않을 때까지 조심하여 가열한 다음 500 ∼ 600 ℃로 강열하여 회화한다. 식힌 다음 염산 2 mL를 넣고 수욕에서 증발건고하고 잔류물을 염산 3 방울로 적시고 열탕 10 mL를 넣어 2 분간 가온한다. 다음에 페놀프탈레인시액 1 방울을 넣고 암모니아시액을 액이 엷은 적색이 될 때까지 적가하고 묽은아세트산 2 mL를 넣어 필요하면 여과하고 물 10 mL로 씻는다. 여액과 씻은 액을 네슬러관에 넣고 물을 넣어 50 mL로 하여 검액으로 한다. 비교액은 질산 2 mL, 황산 5 방울 및 염산 2 mL를 수욕에서 증발하고 다시 수욕에서 증발건고하고 잔류물을 염산 3 방울로 적시고 이하 검액의 조제법과 같은 방법으로 조작한 다음 납표준액 2 mL 및 물을 넣어 50 mL로 한다.
조 작 법 검액 및 비교액에 황화나트륨시액 1 방울씩을 넣어 섞고 직사광선을 피하여 5 분간 방치한 다음 2 개의 관을 흰색의 배경을 써서 네슬러관의 위 또는 옆에서 관찰하여 액의 색을 비교한다. 검액이 나타내는 색은 비교액이 나타내는 색보다 진하지 않다.
29. 질소정량법
가. 킬달법
(1) 장 치
다음 그림과 같다(단위 : mm).
다만, 접속부는 갈아 맞춘 것이라도 좋다.
(2) 조 작 법
따로 규정이 없는 한, 질소 약 20∼30mg에 대응하는 양의 검체를 정밀히 달아 분해플라스크(A)에 넣고 이에 황산칼륨분말 5g, 황산동 0.5g 및 황산 20mL를 가한 다음 플라스크를 약 45°로 기울여 거품이 거의 일어나지 아니할 때까지 조용히 가열하고 다시 온도를 올려서 끓여 내용물이 청색의 투명한 액이 된 다음 다시 1∼2시간 가열한다. 식힌 다음 물 15mL를 천천히 가하여 식히고 이에 비등석 또는 입상의 아연 2∼3립을 가하여 그림과 같이 장치를 한다.
A B C D E F G H | : 분해플라스크(경질유리로 만든 것. 용량 약 500∼800mL) : 유리관 : 알칼리용액주입 깔대기 : 고무관(B와 C를 연결하고 중간에 핀치코크가 있다.) : 와그너관 : 증류관 : 냉각기 : 흡수용플라스크(용량 약300mL) |
흡수용플라스크(H)에는 0.1N 황산 25mL 및 물 약 50mL를 넣고 냉각기(G)의 끝을 이 액 중에 담근 다음 깔대기(C)로 부터 수산화나트륨용액(2→5) 85mL를 천천히 가하고 다시 소량의 물로 씻어 내린 다음 D부분의 핀치코크를 닫고 분해플라스크를 가볍게 흔들어 내용물을 섞은 다음 조용히 가열하고 끓기 시작하면 강하게 가열하여 내용물의 약 3분의 2용량이 유출할 때까지 증류한다.
이어 냉각기의 끝을 흡수용 플라스크의 액면으로부터 조금 떼고 다시 잠시동안 증류를 계속한 다음 냉각기의 끝을 소량의 물로 씻어 내리고 플라스크액중의 과잉의 산을 0.1N 수산화나트륨용액으로 적정한다(지시약 : 브로모크레솔그린ㆍ메틸레드혼합시액 3방울). 따로 같은 방법으로 공시험을 한다.
0.1N 황산 1mL = 1.401mg N
나. 세미마이크로 킬달법
(1) 장 치
경질유리로 만든 것으로서 그 개략은 다음 그림과 같다(단위 : mm). 다만, 접속부는 갈아 맞춘 것이라도 좋다.
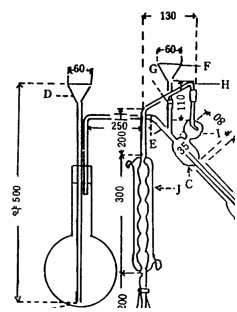
A B C D E F G H I J K L | : 분해플라스크(용량 약 200mL) : 수증기발생기(용량 약 1,000mL) : 와그너관 : 급수깔대기 : 증기관 : 알카리용액 주입깔대기 : 고무관(E와 F를 연결한다. 중간에 핀콕크가 있다) : 도 관 : 작은 구멍(지름은 관의 안지름과 거의 같다) : 냉각기 : 냉각관의 끝 (비스듬히 끊어져 있다) : 흡수용플라스크(용량 약 300mL) |
장치를 계속 조립상태로 둘 때에는 와그너관(C)과 그 부속관을 석면과 탄산마그네슘을 물에 섞은 것을 감아 두는 것이 좋다. 분해플라스크(A)도 천 또는 석면지로 싸서 보온하는 것이 좋다. 증류장치와 분해플라스크 사이의 고무마개에는 글리세린을 발라 둔다. 고무마개 및 고무관은 모두 수산화나트륨시액으로 10분간 끓여 물로 잘 씻고 사용한다. 수증기발생기 (B)에는 물을 넣고 황산 2∼3방울을 가하고 돌비를 방지하기 위하여 비등석을 넣는다. 흡수용플라스크(L)는 사용한 다음 물로 잘 닦고 밀전하여 다음의 시험에 대비한다.
(2) 조 작 법
질소 2∼3mg에 대응하는 양의 검체를 정밀히 달아 분해플라스크(A)에 넣고 이에 분말로 한 황산칼륨 10g 및 황산동 1g의 혼합물 1g을 가한다. 플라스크의 목에 검체가 부착된 경우에는 극히 적은 양의 물로서 씻어 넣는다. 다음 플라스크의 내벽을 따라 황산 7mL를 흘러 내리고 플라스크를 흔들어 움직이면서 과산화수소 1mL를 소량씩 내벽을 따라 주의하여 흘러내린다. 플라스크를 석면금망상에서 가열하여 내용물이 청색의 투명한 액이 되고 플라스크의 내벽에 탄화물이 없을 때 가열을 그친다. 분해가 불충분할 때에는 식힌 다음 다시 과산화수소 소량을 가하여 가열한다.
식힌 다음 물 20mL를 주의하면서 가하여 식히고 플라스크를 미리 수증기를 통하여 씻은 증류장치에 연결한다. 흡수용플라스크(L)에는 붕산용액(1→25) 15mL 및 브로모크레솔그린ㆍ메틸레드혼합시액 3방울을 넣고 물 적당량을 가하여 냉각관의 끝(K)을 이 액 중에 담근다.
깔대기(F)로 부터 수산화나트륨용액(2→5) 30mL를 가하고 다시 물 10mL로 씻어 내린 다음 G부분의 핀치코크를 닫고 즉시 수증기를 통하여 증류를 시작한다.
유출액 80∼100mL를 받고 냉각관의 끝을 액면으로부터 떼어 소량의 물로 그 부분을 씻어 내리고 물을 가하여 157∼180mL로 한 다음 0.01N 황산으로 적정한다.
적정의 종말점 근처에서 액이 거의 무색으로 되었을 때, 다시 브로모크레솔그린ㆍ메틸레드혼합시액 1방울을 넣고 적정을 계속하여 액이 약간 홍색을 나타낼 때를 종말점으로 한다. 따로 같은 방법으로 공시험을 한다.
0.01N 황산 1mL = 0.1401mg N
30. 철시험법
철시험법은 검체중의 불순물로 함유된 철의 한도를 시험하는 방법이다. 그 한도는 철(Fe)로서 중량백만분율(ppm)로 나타낸다.
조 작 법따로 규정이 없는 한 원료각조에서 규정하는 양의 검액(A)을 취하여 묽은질산 5㎖ 및 물을 넣어 45㎖로 하여 검액(B)으로 한다. 따로 원료각조에서 규정하는 양의 철표준액을 취하여 검체를 제외하고 검액(A)와 같이 처리하여 얻은 액을 넣고 여기에 묽은질산 5㎖ 및 물을 넣어 45㎖로 하여 비교액으로 한다. 검액(B) 및 비교액에 치오시안산암모늄시액 5㎖씩을 넣어 흔들어 섞고 5분간 방치한 다음 비색할 때 검액(B)이 나타내는 색은 비교액이 나타내는 색보다 진하지 않다.
31. 황산염시험법
가. 타르색소
황산염시험법은 검체 중에 혼재하는 황산염의 한도시험법으로 그 양의 한도를 황산나트륨 (Na2SO4) 의 %로 나타낸다.
조 작 법 검체 약 2 g을 500 mL 삼각플라스크에 정밀하게 달아 물 약 200 mL를 넣어 녹이고 활성탄 10 g을 넣어 세계 흔들어 녹인 다음 흡인여과한 후 3분간 끓이고 식힌다. 다음에 묽은질산(1 → 2) 1 mL를 넣어 세계 흔들어 녹인 후 흡인여과하고 소량의 물로 씻은 후 그 액에 물을 넣어 250.0 mL로 한다. 이 액을 즉시 양이온교환수지(H형) 5 ∼ 20 mL를 충진한 내경 8 ∼ 15 mm 의 유리관에 1분간 2 ∼ 5 mL의 유속으로 통과시킨다. 처음의 유출액 30 mL는 버리고 다음 유출액을 검액으로 한다. 검액 50 mL를 취하여 묽은염산 1 방울 내지 2 방울을 넣어 끓이고 0.01 mol/L 염화바륨액 10 mL를 정확하게 넣어 몇 분간 끓이고 식힌 후 그 액에 암모니아ㆍ염화암모늄완충액(pH 10.7) 5 mL 및 에틸렌디아민테트라아세트산디나트륨마그네슘사수화물용액(4.3 → 100) 5 mL 및 에리오크롬블랙T 시액 4 방울 내지 5 방울을 넣고, 이 용액의 색이 청자색이 될 때까지 0.01 mol/L 에틸렌디아민테트라아세트산이수소디나트륨시액로 적정한다. 따로 같은 방법으로 공시험하고, 다음의 식에 따라 황산염의 양을 구한다.
b:공시험에 있어서 0.01 mol/L 에틸렌디아민테트라아세트산이수소디나트륨시액의 소비량(mL)
c:0.01 mol/L 에틸렌디아민테트라아세트산이수소디나트륨시액의 소비량(mL)
나. 비타르색소
황산염시험법은 검체 중에 혼재하는 황산염의 한도시험법이다. 그 한도는 황산염 (SO4 로서)의 한도를 %로 ( ) 안에 나타낸다.
조 작 법 따로 규정이 없는 한 의약품각조에서 규정하는 양의 검체를 네슬러관에 넣고 물 적당량에 녹여 40 mL로 한 다음 묽은염산 1 mL 및 물을 넣어 50 mL로 하여 검액으로 한다. 따로 의약품각조에서 규정하는 양의 0.005 mol/L 황산을 취하여 묽은염산 1 mL 및 물을 넣어 50 mL로 하여 비교액으로 한다. 이 때 검액이 맑지 않을 때에는 두 액을 같은 조건으로 여과한다.
검액 및 비교액에 염화바륨시액 2 mL씩을 넣어 섞고 10 분간 방치한 다음 검정색의 배경을 써서 네슬러관의 위 또는 옆에서 관찰하여 혼탁을 비교한다.
검액이 나타내는 혼탁은 비교액이 나타내는 혼탁보다 진하지 않다.
32. 회분시험법
가. 총 회 분
따로 규정이 없는 한 검체 3g을 미리 항량시켜 무게를 달은 도가니에 취하여 550℃에서 검은 탄소가 없어질 때까지 회화시켜 데시케이타에서 식힌 다음 무게를 달아 회분의 양을 구한다. 회화가 완벽하게 되지 않은 경우는 식힌 도가니에 물 1∼2방울을 적신 후 수욕에서 건조 후 다시 회화시킨다.
나. 산불용성회분
가.의 총회분에 따라 얻어진 회분에 묽은염산 25mL를 가하고 5분간 끓여 정량용의 여지를 사용하여 여과하고 잔류물을 뜨거운 물로 충분히 씻고 여지는 건조, 회화하여 회분량을 구한 후 여지의 회분량을 제외하여 산불용성회분의 양으로 한다.
33. 흡광도측정법
흡광도측정법은 검체가 일정한 좁은 파장범위의 빛을 흡수하는 정도를 측정하는 방법이다. 물질의 용액의 가시부 및 자외부흡수스펙트럼은 그 물질의 화학구조에 따라 정하여진다.
그러므로 여러가지 파장에 있어서의 흡수를 측정하여 물질을 확인할 수 있다. 보통 흡수의 극대파장(λmax) 또는 극소파장(λmin)에 있어서의 일정한 농도용액의 흡광도를 측정하여 확인시험, 순도시험 및 정량시험을 한다.
단색광이 어떤 물질용액을 통과할 때, 투과광의 강도(I)와 입사광의 강도(I0)와의 비를 투과도(T)라 하고, 투과도의 역수의 상용대수를 흡광도(A)라 한다.
T = | I |
I0 |
A = | log | I0 | = - log T |
I |
흡광도(A)는 용액의 농도(c) 및 액층의 길이(l)에 비례한다.
A =kc l
l을 1cm, c를 1%용액으로 환산한 때의 흡광도를, l을 1cm, c를 1M용액으로 환산한 때의
흡광도를 분자흡광계수(E)라 한다.
흡수의 극대파장에 있어서의 분자흡광계수는 Emax로 표시 한다
흡광도측정은 규정된 용매를 쓴 용액에 대하여 시험한다. 용액의 농도는 측정에서 얻은 흡광도가 0.2∼0.7의 범위가 되는 것이 적당하므로 용액의 흡광도가 이보다 높을 때에는 적당한 농도가 되도록 용매로 희석한 다음 측정한다. 또는 E를 구할 때는 다음 계산식에 따른다.
| = | a |
c(%) × l |
E | = | a |
c(mol) × l |
l : 액층의 길이(cm)
a : 측정에서 얻은 흡광도
c(%) : 검체용액의 농도(w/v%)
c(mol) : 검체용액의 농도(mol)
가. 장치 및 조제법
측정장치로서 광전분광광도계 또는 광전비색계를 쓴다. 광전분광광도계는 모노크로미이터와 광전광도계를 구비한 것으로서, 광원으로는 텅스텐램프 또는 수소방전관을 쓰며 각각 가시부 및 자외부의 흡수를 측정한다. 광전비색계는 광학적필터와 광전광도계를 구비한 것으로서, 광원으로는 텅스텐램프를 써서 가시부의 흡수를 측정한다. 큐벳트는 자외부흡수측정에는 석영제, 가시부흡수측정에는 유리제를 쓴다.
우선 각각의 시험법에 표시되어 있는 필터 또는 정하여진 측정파장을 중심투과파장으로 하는 필터를 써서 분광광도계의 파장눈금을 측정파장에 맞추어 대조액을 광로에 넣고 조절하여 흡광도를 0이 되도록 한 다음 측정하고자 하는 용액을 광로에 바꾸어 넣고 이때에 나타나는 흡광도를 읽는다. 필터는 될 수 있는 대로 그 중심투과파장이 용액의 흡수의 극대파장과 일치하고 필터투과과정의 파장폭이 흡수대의 폭보다 좁은 것을 택하는 것이 좋다.
각 품목중의 흡광도의 항에서 “공시험을 하여 보정한다”라고 기재한 것은 대조액으로서 검체를 쓰지 아니하고 위와 같이 조작한 액을 쓰는 것을 말하며, “용매를 대조로 하여 공시험을 한다”라고 기재한 것은 대조액으로서 검체용액에 쓰인 용매와 같은 것을 쓰는 것을 말한다.
나. 흡광도측정에 의한 물질의 정량법
흡광도(A)를 표시하는 위의 식은 람베르트‧베어의 법칙이라 하는 것으로서, 이 법칙은 보통 검체의 어느 일정한 농도범위에서 성립되는 것이므로 흡광도측정에 의하여 물질의 정량을 할 때에는 미리 측정 가능한 농도범위를 알 필요가 있다.
특히 표준용액이 정하여져 있지 아니할 때에는 검체의 순품을 써서 각종 농도의 용액을 만들어 위와 같이 흡광도를 측정하여 흡광도와 성분량(농도)과의 관계곡선을 만들 때, 베어의 법칙이 성립하는 범위에서는 직선이 되므로 이를 검량선으로 하여 정량한다.
다. 파장 및 흡광도눈금의 검정
파장눈금은 보통 석영수은등 또는 유리수은등 239.95, 253.65, 302.16, 313.16, 334.15, 365.48, 404.66, 435.83, 546.10nm 및 수소방전관 486.13, 656.28nm의 파장을 써서 검정한다. 흡광도눈금은 중크롬산칼륨(표준시약)을 0.01N 황산에 녹여 0.006w/v%로 한 액을 써서 검정한다.
이 액의 파장 235(극소), 257(극대), 313(극소) 및 350nm(극대)에 있어서 각 125.2, 145.6, 48.9 및 107.0이다.
34. pH측정법
장 치 pH 측정기는 유리전극 및 참조전극으로 된 검출부와 검출된 기전력을 증폭하는 증폭부 및 측정결과를 표시하는 지시부로 되어 있다. 지시부에는 영점교정용 및 감도조정용 다이얼이 있다. 그 밖에 장치에 따라서는 온도보상용 다이얼이 있는 것도 있다. pH 측정기는 다음 조작법에 따라 임의의 한 종류의 pH 표준액의 pH를 매회 검출부를 물로 잘 씻은 다음 5 회 반복하여 측정할 때 지시한 값의 재현성이 ± 0.05 이내 인 것을 쓴다.
조 작 법 유리전극은 미리 물에 수 시간 이상 담가 둔다. pH 측정기는 전원을 넣어 5분 이상 장치가 안정된 것을 확인한 다음에 쓴다. 검출부를 물로 잘 씻고 부착된 물은 여과지 등으로 가볍게 닦아 낸다.
pH 측정기의 교정을 1 종류의 pH 표준액을 써서 하는 경우는 온도보상용 다이얼이 있는 장치를 쓰는 경우 눈금 값을 pH 표준액의 온도에 일치시킨 다음 교정한다. 검출부를 검체용액의 pH 값에 근접한 pH 표준액에 담그고 2 분 이상 지난 후 pH 의 지시가 그 온도에 일치하지 않을 경우에는 온도보상용 다이얼로 규정하는 pH에 일치시킨다.
pH 측정기의 교정은 2 종류의 pH 표준액을 써서 보통 다음과 같이 한다. 전극을 인산염 pH 표준액에 담그고 영점교정용다이얼로 표의 pH에 일치시킨다. 다음에 예상되는 검액의 pH에 가까운 pH를 갖는 pH 표준액을 두 번째 표준액으로 하여 같은 조건으로 pH를 측정한다. 얻어진 pH가 표에 나타낸 pH와 일치하지 않을 때에는 감도교정용다이얼로 규정하는 pH에 일치시킨다. 두 종류의 pH 표준액의 pH가 조정하지 않고도 규정하는 pH의 ± 0.05 pH 단위에 일치할 때까지 같은 조작을 반복한다. 또 온도보상용다이얼이 있는 장치를 쓰는 경우 눈금 값을 pH 표준액의 온도에 일치시킨 다음 교정한다. 장치의 교정이 끝난 다음 검출부를 물로 잘 씻고 여과지 등으로 가볍게 닦아낸다.
pH표준액 pH표준액의 조제에 사용하는 물은 정제수를 증류해 유액을 15분 이상 끓인 후 이산화탄소흡수관(소오다석회)으로 냉각한다. pH 경질 유리병 또는 폴리에틸렌 병에 밀폐하여 보관한다.
1) 수산염 pH표준액 pH측정용 이수산삼수소칼륨이수화물을 분말로 하여 데시케이터(실리카겔)로 건조시키고 그 12.71 g(0.05 mol)을 정밀히 달아 물에 녹여서 정확히 1 L로 한다.
2) 프탈산염 pH표준액 pH측정용 프탈산수소칼륨을 분말로 하여 110 ℃에서 항량이 될 때 까지 건조시키고 그 10.21 g(0.05 mol)을 정밀히 달아 물에 녹여서 정확히 1 L로 한다.
3) 인산염 pH표준액 pH측정용 인산이수소칼륨 및 pH측정용 인산수소이나트륨을 분말로 하여 110 ℃에서 항량이 될 때까지 건조시키고 인산이수소칼륨 3.40 g(0.025 mol) 및 인산수소이나트륨 3.55 g(0.025 mol)을 정밀히 달아 물에 녹여서 정확히 1 L로 한다.
4) 붕산염 pH표준액 pH측정용 사붕산나트륨십수화물을 데시케이터(브롬화나트륨포화용액) 속에 방치해 항량으로 한 후 그 3.81 g(0.01 mol)을 정밀히 달아 물에 녹여서 정확히 1 L으로 한다.
5) 탄산염 pH표준액 pH측정용 탄산수소나트륨을 데시케이터(실리카겔)로 항량이 될 때 까지 건조시키고 그 2.10 g(0.025 mol)을 정밀히 단 것 및 pH측정용 탄산나트륨을 300 ℃이상 500 ℃이하로 항량이 될 때 까지 건조시키고 그 2.65 g(0.025 mol)을 정밀히 단 것을 물에 녹여서 정확히 1 L로 한다.
6) 수산화칼슘 pH표준액 pH측정용 수산화칼슘을 분말로 하고 그 5 g을 플라스크에 달아 물 1 L를 넣어 잘 흔들어 섞어 23 ℃이상 27 ℃이하로 하고 충분히 포화한 후 그 온도에서 상등액을 여과하고 맑고 투명한 여액 (약 0.02 mol/L)을 사용한다.
이것의 pH표준액의 명 온도에 있어 pH값을 다음의 표에 나타낸다. 이 표에 없는 온도의 pH값은 표의 값부터 내삽법에 따라구한다.
[6종의 pH 표준액에 대한 온도 의존성]
온 도 (℃) | 수 산 염 pH 표준액 | 프탈산염 pH 표준액 | 인 산 염 pH 표준액 | 붕 산 염 pH 표준액 | 탄 산 염 pH 표준액 | 수산화칼슘 pH 표준액 |
0 5 10 15 20 25 30 35 40 50 60 | 1.67 1.67 1.67 1.67 1.68 1.68 1.69 1.69 1.70 1.71 1.73 | 4.01 4.01 4.00 4.00 4.00 4.01 4.01 4.02 4.03 4.06 4.10 | 6.98 6.95 6.92 6.90 6.88 6.86 6.85 6.84 6.84 6.83 6.84 | 9.46 9.39 9.33 9.27 9.22 9.18 9.14 9.10 9.07 9.01 8.96 | 10.32 10.25 10.18 10.12 10.07 10.02 9.97 9.93 | 13.43 13.21 13.00 12.81 12.63 12.45 12.30 12.14 11.99 11.70 11.45 |
35. 시약・시액・표준액・용량분석용 표준액・박층크로마토그래프용 표준품・계량기・용기
1) 시약ㆍ시액, 표준액, 용량분석용 표준액
과망간산칼륨 KMnO4 [최순품]
과망간산칼륨시액 과망간산칼륨 3.3 g을 물에 녹여 1 L 용액으로 만든다 (0.02 mol/L).
과산화수소(30) H2O2 [최순품, 농도 30.0 ∼ 35.5 %]
과산화수소시액 과산화수소(30) 1 용량에 물 9 용량을 넣는다. 쓸 때 만든다 (3 %).
과염소산 HClO4 [최순품, 비중 약 1.67, 밀도 1.67 g/mL, 농도 70.0 % ∼ 72.0 %]
과염소산바륨(Barium Perchlorate) Ba(ClO4)2 [최순품]
0.005mol/L 과염소산바륨액 1000mL중 과염소산바륨[Ba(ClO4)2:336.24] 1.6812g을 함유한다.
1) 조제 과염소산바륨 1.7g에 물 20mL를 넣어 녹여 이소프로판올을 넣어 1L로 하고 다음과 같이 표정한다.
2) 표정 미리 만든 과염소산바륨액 20mL를 정확하게 취하여 메탄올 55㎖ 및 알세나조Ⅲ시액 0.15mL를 넣어 0.005mol/L 황산으로 액의 자색이 적자색을 거쳐 적색을 나타낼 때까지 적정하여 규정도계수를 계산한다.
0.0025 mol/L 과염소산바륨액 1000mL 중 과염소산바륨[Ba(ClO4)2:336.24] 0.8406g을 함유한다. 쓸 때 0.005 mol/L 과염소산바륨액에 물을 넣어 정확하게 2 배 용량으로 한다.
구연산암모늄 (NH4)2HC6H5O7 [디구연산암모늄, 특급]
구연산암모늄시액 구연산암모늄 10g을 물에 녹여 100mL로 한다.
글리세린 C3H8O3 [대한민국약전 의약품 각조, ‘농글리세린’]
납표준액 납표준원액 10 mL를 정확하게 달아 물을 넣어 정확히 100 mL로 한 용액으로 이 액 1 mL은 납(Pb) 0.01 mg을 함유한다. 쓸 때 만든다.
납표준원액 질산납(II) 0.1598 g을 정밀하게 달아 묽은질산 10 mL에 녹여 물을 넣어 정확하게 1 L로 한 용액으로, 이 액의 조제 및 보존은 가용성납염을 함유하지 않는 유리용기를 쓴다.
납표준원액 (원자흡광광도법용) 질산납(II) 1.598 g을 정밀하게 달아 묽은질산 100 mL에 녹여 물을 넣어 정확하게 1 L로 한 용액으로, 이 액의 조제 및 보존은 가용성납염을 함유하지 않는 유리용기를 쓴다.
니트로벤젠 C6H5NO2 [최순품]
β-니트로소-α-나프톨 C10H7NO2 [2-니트로소-1-나프톨] 황색의 침상결정. 에탄올(95), 아세트산(100) 및 에 잘 녹고, 에텔, 벤젠, 클로로포름 및 석유에텔에는 녹기 어렵다. 융점은 162 ∼ 164 ℃ 이다.
2, 2’, 2’’-니트릴트리에탄올 (CH2CH2OH)3N [순품]
디메틸설폭시드 (CH3)2SO [최순품]
N,N-디에틸디티오카르바미드은 C5H10AgNS2 [최순품]
N,N-디에틸디티오카르바민산나트륨삼수화물 (C2H5)2NCS2Naㆍ3H2O [최순품]
1,2-디클로로에탄 ClCH2CH2Cl [최순품]
2,2'-디피리딜 C10H8N2 [최순품]
α,α'-디피리딜 2,2'-디피리딜 참조.
리트머스시험지, 적색 [적색리트머스시험지]
리트머스시험지, 청색 [청색리트머스시험지]
만델산 C8H8O3 [α―옥시페닐아세트산]무색의 판상 결정이다. 융점은 133 ℃ 이다.
망간표준원액 (원자흡광광도법용) [망간표준액(Mn1000)]
메탄올 CH3OH [최순품]
메틸레드 C15H15N3O2 [최순품] 변색범위는 pH 4.2 (적색)부터 6.2 (황색)까지이다.
메틸레드시액 메틸레드 0.1 g을 에탄올(95) 100 mL에 녹여 필요하다면 여과한 것으로 한다.
3-메틸-1-부탄올 C5H12O [최순품]
메틸옐로우 C14H15N3 [최순품]
메틸옐로우시액 메틸옐로우 0.1 g에 에탄올(95) 200 mL를 넣어 녹인다.
메틸오렌지 C14H14N3NaO3S [최순품] 변색범위는 pH 3.1 (적색)부터 4.4 (등황색)까지이다.
메틸오렌지시액 메틸오렌지 0.1 g을 물 100 mL에 녹여 필요하다면 여과한 것으로 한다.
4-메틸-2-펜타논 CH3COCH2CH(CH3)2 [최순품]
몰리브덴산암모늄시액 칠몰리브덴산육암모늄사수화물 21.2 g에 물을 넣어 녹여 200 mL로 한다 (10 %). 쓸 때 만든다.
1-부탄올 CH3(CH2)2CH2OH [최순품]
벤젠 C6H6 [최순품]
붕산 H3BO3 [최순품]
브롬시액 브롬(Br)을 물에 포화시켜 조제한 용액으로 뚜껑에 바셀린을 발라 마개가 있는 병에 브롬 2 ∼ 3 mL를 넣고 차가운 물 100 mL를 넣어 뚜껑을 잘 닫아 흔들어 섞어 만든다. 차광하여 냉소에서 보관한다.
브롬티몰블루 C27H28Br2O5S [최순품] 변색범위는 pH 6.0 (황색)에서 7.6 (청색)까지이다.
브롬티몰블루시액 브롬티몰블루 0.1 g을 묽은에탄올 100 mL에 녹이고 필요하다면 여과한 용액으로 한다.
브롬크레솔그린 C21H14Br4O5S [최순품] 변색범위는 pH 3.8 (황색)에서 5.4 (청색)까지이다.
브롬크레솔그린시액 브롬크레솔그린 0.05 g을 에탄올(95) 100 mL에 녹이고 필요하다면 여과한 용액으로 한다.
브롬화나트륨 NaBr [최순품]
브롬화칼륨 (적외흡수스펙트럼측정용) 브롬화칼륨 단결정 및 브롬화칼륨을 곱게 갈아 200호 (75 μm)체를 통과한 가루를 모아 120 ℃에서 10 시간 또는 500 ℃에서 5 시간 건조한 것으로 이를 이용하여 정제를 만들어 적외흡수스펙트럼측정법으로 측정할 때 특이한 흡수를 보이지 않는다.
브롬ㆍ브롬화칼륨시액 브롬 30g 및 브롬화칼륨 30g을 물에 녹여 100mL로 한다.
비소표준액 비소표준원액 10 mL를 정확히 달아 묽은황산 10 mL를 넣고 새로 증류하여 냉각한 물을 넣어 정확히 1 L로 한 것으로 1 mL당 삼산화비소(As2O3) 1 μg을 함유하는 용액으로 한다. 쓸 때 만들고 마개가 있는 병에 보관한다.
비소표준원액 삼산화비소 (표준시약)을 미세한 가루로 하여 105 ℃에서 4 시간 건조하고, 그 중 0.100 g을 정밀하게 달아 수산화나트륨용액(1 → 5) 5 mL에 녹이고 묽은황산을 넣고 중화한 다음 묽은황산 10 mL를 더 넣고 새로 증류하고 냉각한 물을 넣어 정확히 1 L 용액으로 만든다. 마개가 있는 병에 보관한다.
비스무트산나트륨 삼산화비스무트나트륨 참조.
비화수소흡수액 N,N-디에틸디티오카르바미드은 0.05 g을 피리딘에 녹여 100 mL 용액으로 만든다. 이 액은 차광하여 마개가 있는 병에 넣어 냉소에 보관한다.
삼산화비소 (표준시약) As2O3 [삼산화비소, 용량분석용표준물질]
삼산화비스무트나트륨 NaBiO3 황갈색의 가루이다.
확인시험
(1) 이 약 10 mg을 취하여 질산망간(II)용액(4 → 125) 5 mL 및 묽은질산(1 → 3) 1 mL를 넣고 10 초간 세게 흔들어 섞을 때 액은 자주색을 나타낸다.
(2) 이 약 10 mg을 취하여 묽은염산(1 → 2) 2 mL에 녹인 액은 나트륨염의 정성반응(1)을 나타낸다.
석유에텔 [최순품]
설포살리실산시액 설포살리실산이수화물 5 g에 물을 넣어 녹여 100 mL로 한다.
소오다석회 [이산화탄소흡수용]
수산암모늄일수화물 (NH4)2C2O4ㆍH2O [최순품]
수산화나트륨 NaOH [최순품]
수산화나트륨시액 수산화나트륨 4.3 g을 물에 녹여 100 mL 용액으로 만들고 (1 mol/L), 폴리에틸렌병에 보관한다.
수산화나트륨시액, 묽은 수산화나트륨 4.3 g에 새로 증류하여 냉각한 물을 넣어 녹여 1 L 용액(0.1 mol/L)으로 하고, 쓸 때 만든다.
0.1 mol/L 수산화나트륨액 1000 mL 중 수산화나트륨 (NaOH : 39.997) 3.9997 g을 함유하는 용액으로 다음 규정에 따른다.
1) 조제 수산화나트륨 4.5 g을 달아 1 mol/L 수산화나트륨액에 따라 만들어 다음과 같이 표정한다.
2) 표정 1 mol/L 수산화나트륨액에 따른다. 다만 아미도황산 (표준시약) 약 0.25 g을 정밀하게 달아 적정한다.
0.1 mol/L 수산화나트륨액 1 mL= 9.709 mg HOSO2NH2
주의 : 1 mol/L 수산화나트륨액에 따라 보존한다. 오랫동안 보존한 것은 다시 표정하여 쓴다.
수산화칼륨 KOH [최순품]
0.1 mol/L 수산화칼륨액 1000 mL 중 수산화칼륨 (KOH : 56.11) 5.611 g을 함유한다.
1) 조제 수산화칼륨 6.5 g을 달아 1 mol/L 수산화칼륨액에 따라 만들어 다음과 같이 표정한다.
2) 표정 1 mol/L 수산화칼륨액에 따른다. 다만 아미도황산 (표준시약) 약 0.25 g을 정밀하게 달아 적정한다.
0.1 mol/L 수산화칼륨액 1 mL = 9.709 mg HOSO2NH2
주의 : 1 mol/L 수산화칼륨액에 따라 보존한다. 오랫동안 보존한 것은 다시 표정하여 쓴다.
수은표준원액 염화수은(Ⅱ)을 데시케이터 (실리카겔)에서 6 시간 건조하여 13.5 mg을 정확하게 달아 묽은질산 10 mL 및 물을 넣어 녹여 정확하게 1000 mL로 한다. 쓸 때 만든다. 이 액 1 mL는 수은 (Hg) 10 μg을 함유한다.
시안화칼륨 KCN [최순품]
시안화칼륨시액 시안화칼륨 1 g에 물을 넣어 녹여 10 mL로 한다. 쓸 때 만든다.
시클로헥산 C6H12 [최순품]
시트르산수소이암모늄 C6H14N2O7 [최순품]
실리카겔 무정형의 일부 수가성의 규산으로 부정형의 유리상과립이다. 건조제용으로 수분흡착에 의하여 변색하는 변색료를 포함시킨 것도 있다. 110 ℃에서 건조되어 원래의 색으로 되돌아온다.
1) 강열감량 : 6 % 이하 (2 g, 950 ± 50 ℃)
2) 수분흡착능 : 31 % 이상. 이 약 약 10 g을 칭량병에 정밀하게 달아 뚜껑을 열고 비중 1.19의 황 산으로 습도를 80 %로 한 용기내에 24시간 둔 다음 질량을 달아 검체에 대한 증량을 구한다.
실리카겔 (박층크로마토그래프용) 실리카겔로 박층크로마토그래프용으로 제조된 것을 사용한다.
실리콘유 무색투명한 액으로 냄새는 없다. 점도 50 ∼ 100 mm2/S
아세톤 CH3COCH3 [최순품]
아세트산(100) CH3COOH [아세트산, 최순품]
아세트산, 묽은 아세트산(100) 6 g에 물을 넣어 100 mL 용액으로 만든다 (1 mol/L).
아세트산나트륨삼수화물 CH3COONaㆍ3H2O [최순품]
아세트산나트륨시액 아세트산나트륨삼수화물 13.6 g을 물에 녹여 100 mL 용액으로 만든다 (1 mol/L).
아세트산납(II)삼수화물 Pb(CH3COO)2ㆍ3H2O [최순품]
아세트산납시액 아세트산납(II)삼수화물 9.5 g에 새로 증류하여 냉각한 물을 넣어 녹이고 100 mL 용액으로 만든다 (0.25 mol/L). 밀전하여 보관한다.
아세트산ㆍ아세트산나트륨시액 수산화나트륨시액 17 mL에 묽은아세트산 40 mL와 물을 넣어 100 mL 용액으로 만든다.
아세트산ㆍ아세트산나트륨완충액 아세트산나트륨시액에 묽은아세트산을 넣고 pH 6.0으로 조정한 용액으로 만든다 (1 mol/L).
아세트산ㆍ아세트산나트륨완충액, pH 4.5, 철시험용 아세트산(100) 75.4 mL 및 아세트산나트륨삼수화물 111 g을 물에 녹여 1000 mL로 한다.
아세트산암모늄 CH3COONH4 [아세트산, 최순품]
아세트산암모늄시액 아세트산암모늄 1.54 g을 물에 녹여 1 L 용액으로 만든다 (0.02 mol/L).
아스코르브산 L-아스코르브산 참조.
아스코르브산, 철시험용 L-아스코르브산 참조.
L-아스코르브산 C6H8O6 [L(+)-아스코르브산, 최순품]
아연 (표준시약) Zn [용량분석용 표준물질]
아연 (비소분석용) Zn [비소분석용] 입자경이 약 800 μm인 것.
아연가루 Zn [비소분석용]
아연표준액 아연표준원액 50 mL를 정확하게 취하여 물을 넣어 정확히 1 L로 하며, 쓸 때 만든다. 이 액 1 mL는 아연 (Zn) 0.05 mg를 함유한다.
아연표준원액 아연 (표준시약) 1.000 g을 정밀히 달아, 물 100 mL와 염산 5 mL를 넣고 서서히 가열 하여 녹이고 상온이 될 때까지 식힌 다음 물을 넣어 1 L로 만든다.
아연표준원액 (원자흡광광도법용) 아연(표준시약) 1.000 g을 정밀히 달아, 물 100 mL와 염산 5 mL를 넣고 서서히 가열하여 녹이고 상온이 될 때까지 식힌 다음 물을 넣어 1 L로 만든다.
아황산나트륨 NaSO3 [특급]
아황산나트륨, 무수 Na2SO3 [특급]
아황산나트륨시액, 납시험법용 아황산나트륨 15g에 물을 넣어 100㎖로 한다. 쓸 때 만든다.
아황산나트륨시액, 중화 무수아황산나트륨 30g에 물 100㎖를 넣어 녹이고 여기에 페놀프탈레인시액 2방울을 넣어 아세트산로 중화한다.
알리자린 S 알리자린레드 S 참조.
알리자린 S 시액 알리자린레드 S 시액 참조.
알리자린레드 S C14H7NaO7SㆍH2O [최순품]
알리자린레드 S 시액 알리자린레드 S 0.1 g에 물을 넣어 녹여 100 mL로 한다. 필요하면 여과한다.
알세나조Ⅲ(Arsenazo Ⅲ) C22H16As2N4Na2O12S2 어두운 적색의 가루로 물 및 수산화나트륨시액에 녹기 쉽고 아세톤에는 거의 녹지 않는다. 감도:이 원료의 수용액(1→100) 0.5mL에 물 50mL 및 에탄올 50mL를 넣고 0.005 mol/L 과염소산바륨액 0.1mL를 넣을 때 액은 청자색을 나타내고 여기에 0.005mo/L 황산 0.2mL를 넣을 때 적색으로 변한다.
암모니아수(28) NH3 [암모니아수, 최순품, 비중 약 0.90, 밀도 0.908 g/mL, 함량 28 % ∼ 30 %]
암모니아시액 암모니아수(28) 400 mL에 물을 넣어 1 L로 만든다. (함유율이 약 10 %가 되는 것)
암모니아시액, 묽은 암모니아수(28) 3 mL에 물을 넣어 100 mL로 만든다.
암모니아ㆍ염화암모늄완충액, pH 10.7 염화암모늄 67.5 g을 물에 녹여 암모니아수 (28) 570 mL를 넣고, 물을 넣어 1 L로 만든다.
양이온교환수지 폴리스틸렌설폰산의 나트륨염으로 분말도는 26호(600 μm)체를 통과하고 36호(425 μm)체를 대부분 통과하지 않는 것으로 다음과 같이 조제된 것으로 담황색에서 황갈색까지의 색을 나타낸다. 이 약 약 50 g을 달아 물에 30 분간 담근 후, 내경 약 2.5 cm의 크로마토그래프용 유리관에 물과 같이 흘려 보내 수지기둥을 만든다. 여기에 묽은염산(1 → 4) 250 mL를 1 분간 약 4 mL의 속도로 흘려 보낸 후 세액이 브롬크레솔그린시액으로 녹색부터 청색까지의 색을 나타낼 때까지 물로 씻고 다음을 확인한다. 이 수지 10 mL를 달아 내경 1.5 cm의 크로마토그래프용 유리관에 물과 같이 흘려 보내 수산화나트륨시액(묽은) 80 mL를 1 분간 약 2 mL의 속도로 흘려보낸 액의 pH가 5.0부터 6.5까지인 것으로 한다.
에리오크롬블랙T C20H12N3O7SNa [최순품]
에리오크롬블랙T시액 에리오크롬블랙T 0.3 g 및 염산히드록실암모늄 2 g에 메탄올을 넣고 녹여 50 mL 용액으로 만든다. 차광보관하고 조제 후 1주일 이내에 사용한다.
에리오크롬블랙Tㆍ염화나트륨지시약 에리오크롬블랙T 0.1 g 및 염화나트륨(NaCl)[최순품] 10 g을 섞어 균질하게 될 때까지 빻은 것으로 한다.
에탄올(95) C2H5OH [최순품]
에탄올(99.5) C2H5OH [최순품]
에탄올, 묽은 에탄올(95) 1용량에 물 1용량을 넣어 만들며, C2H5OH로서 47.45 vol% ∼ 50.00 vol%를 함유한다.
에탄올, 묽은산성 묽은염산(23.6 → 250) 250 mL에 에탄올(99.5) 250 mL를 넣은 것으로 한다.
에탄올ㆍ에테르시액, 중화(AlcoholㆍEther TS, Neutralized) 에탄올 및 에텔의 같은 용량의 혼합액 적당량에 페놀프탈레인시액 3방울을 넣고 여기에 0.1mol/L 수산화칼륨ㆍ에탄올액을 액이 홍색을 나타낼 때까지 넣는다. 쓸 때 만든다.
아세트산에틸 CH3COOC2H5 [최순품]
에테르 C2H5OC2H5(에틸에테르) [최순품]
에틸렌글리콜 HOCH2CH2OH [최순품]
에틸렌디아민테트라아세트산디나트륨마그네슘사수화물 C10H12N2O8MgNa2ㆍ4H2O 흰색가루이며 이 약 1 g에 물을 넣어 초음파를 사용하여 녹인 것으로 전체량을 100 mL로 한 용액은 무색 투명하고 pH는 8.0 ∼ 9.5이다. 이 용액 5 mL에 물 100 mL, 암모니아ㆍ염화암모늄완충액 (pH 10.7) 2 mL 및 에리오크롬블랙T시액을 한, 두 방울 떨어뜨리면 청자색으로 색이 변하고, 또한 이 용액에 0.01 mol/L 에틸렌디아민테트라아세트산이수소디나트륨시액 0.05 mL를 넣으면 청색으로 색이 변한다.
0.02 mol/L 에틸렌디아민테트라아세트산이수소디나트륨시액 1 L 중 에틸렌디아민테트라아세트산이수소디나트륨이수화물 (C10H14N2Na2O8ㆍ2H2O : 372.24) 7.445 g을 함유하는 용액으로 다음 규정에 따른다.
1) 조제 : 에틸렌디아민테트라아세트산이수소디나트륨이수화물 7.5 g을 물에 녹여 1 L로 하고 표정한다.
2) 표정 : 아연(표준시약)을 묽은염산으로 씻은 후, 물로 씻고, 으로 씻은 후 110 ℃로 5 분간 건조하고 데시케이터(실리카겔)에 넣어 식힌 후, 이 약 0.3 g을 정밀히 달아 묽은염산 5 mL 및 브롬시액 5 방울을 넣고 서서히 가온하여 녹인 후, 증류하여 과량의 브롬을 제거하고 물을 가하여 정확히 200 mL로 한다. 이 액 20 mL를 정확히 달아 수산화나트륨용액(1 → 50)을 넣고 중성으로 하고 암모니아ㆍ염화암모늄완충액 (pH 10.7) 5 mL 및 에리오크롬블랙T시액ㆍ염화나트륨지시약 0.04 g을 넣고 조제한 0.02 mol/L 에틸렌디아민테트라아세트산이수소디나트륨시액으로 액이 적자색에서 청자색으로 변할 때까지 적정하여 계수를 계산한다.
0.02 mol/L 에틸렌디아민테트라아세트산이수소디나트륨 1 mL = 1.3078 mg Zn
3) 저장법 : 폴리에틸렌병에 저장한다.
0.01 mol/L 에틸렌디아민테트라아세트산이수소디나트륨시액 1 L 중 에틸렌디아민테트라아세트산이수소디나트륨이수화물(C10H14N2Na2O8ㆍ2H2O : 372.24) 3.7224 g을 함유하는 용액으로 만들며, 용시 0.02 mol/L 에틸렌디아민테트라아세트산이수소디나트륨에 물을 넣어 정확히 2배 용량이 되도록 조제한 것.
에틸렌디아민테트라아세트산이수소디나트륨이수화물 C10H14N2Na2O8ㆍ2H2O [최순품]
염산 HCl [최순품]
염산, 묽은 염산 23.6 mL에 물을 넣어 100 mL 용액으로 만든다 (10 %).
2 mol/L 염산 1000 mL 중 염산 (HCl : 36.461) 72.92 g을 함유한다.
1) 조제 염산 180 mL 에 물을 넣어 1000 mL로 하고 다음과 같이 표정한다.
2) 표정 1 mol/L 염산에 따른다. 다만 탄산나트륨 (표준시약) 약 2.6 g을 정밀하게 달아 물 100 mL를 넣어 녹여 적정한다.
2 mol/L 염산 1 mL = 105.99 mg Na2CO3
1 mol/L 염산 1000 mL 중 염산 (HCl : 36.461) 36.461 g을 함유한다.
1) 조제 염산 90 mL에 물을 넣어 1000 mL로 하고 다음과 같이 표정한다.
2) 표정 탄산나트륨 (표준시약)을 500 ∼ 650 ℃에서 40 ∼ 50 분간 가열하고 데시케이터 (실리카겔)에서 방랭한 다음 약 1.3 g을 정밀하게 달아 물 50 mL를 넣어 녹여 메틸레드시액 3 방울을 넣고 조제된 염산으로 적정하여 규정도계수를 계산한다. 다만, 적정의 종말점은 용액을 조심하여 끓이고 가볍게 마개를 하여 식힐 때 지속적인 주황색 ∼ 등적색을 나타낼 때로 한다.
1 mol/L 염산 1 mL = 52.99 mg Na2CO3
0.5 mol/L 염산 1000 mL 중 염산 (HCl : 36.461) 18.230 g을 함유한다.
1) 조제 염산 45 mL에 물을 넣어 1000 mL로 하고 다음과 같이 표정한다.
2) 표정 1 mol/L 염산에 따른다. 다만 탄산나트륨 (표준시약) 약 0.7 g을 정밀하게 달아 물 50 mL를 넣어 녹여 적정한다.
0.5 mol/L 염산 1 mL = 26.497 mg Na2CO3
0.1 mol/L 염산 1000 mL 중 염산 (HCl : 36.461) 3.6461 g을 함유한다.
1) 조제 염산 9.0 mL 에 물을 넣어 1000 mL로 하고 다음과 같이 표정한다.
2) 표정 1 mol/L 염산에 따른다. 다만 탄산나트륨 (표준시약) 약 0.15 g을 정밀하게 달아 물 30 mL를 넣어 녹여 적정한다.
0.1 mol/L 염산 1 mL = 5.299 mg Na2CO3
0.01 mol/L 염산 1000 mL 중 염산 (HCl : 36.461) 0.36461 g을 함유한다. 쓸 때 0.1 mol/L 염산에 물을 넣어 정확하게 10 배 용량으로 한다.
0.02 mol/L 염산 1000 mL 중 염산 (HCl : 36.461) 0.7292 g을 함유한다. 쓸 때 0.1 mol/L 염산에 물을 넣어 정확하게 5 배 용량으로 한다.
염산시액, 6 mol/L 염산 540 mL에 물을 넣어 1000 mL로 한다.
염산시액, 0.06 mol/L 1 mol/L 염산시액 60 mL에 물을 넣어 1000 mL로 한다.
염산히드록실암모늄 NH2OHㆍHCl [최순품]
염화나트륨(표준시약) NaCl [용량분석용표준물질]
염화바륨이수화물 BaCl2ㆍ2H2O [최순품]
염화바륨시액 염화바륨이수화물 12 g에 물을 넣어 녹여 100 mL로 한다 (0.5 mol/L).
0.01 mol/L 염화바륨액 1 L 중 염화바륨이수화물(BaCl2ㆍ2H2O : 244.26) 2.4426 g을 함유하는 용액으로 만들고, 쓸 때 0.02 mol/L 염화바륨액에 물을 넣어 정확하게 2배 용량이 되도록 조제한다.
0.02 mol/L 염화바륨액 1 L 중 염화바륨이수화물(BaCl2ㆍ2H2O : 244.26) 4.885 g을 함유하는 용액으로 다음 규정에 따른다.
1) 조제 : 염화바륨이수화물 4.9 g을 물에 녹여 1 L로 하고 다음 방법으로 표정한다.
2) 표정 : 조제한 염화바륨액 100 mL를 정확히 달아 염산 3 mL를 넣고 가온한다. 미리 가온해 놓은 묽은황산(1 → 130) 40 mL를 넣고 수욕에서 30분간 가열한 뒤 그대로 둔다. 다음 날 이 액을 여과하여 여지위의 잔류물을 여액에 질산은시액을 넣어도 혼탁해지지 않을 때까지 물로 씻어 여지와 같이 도가니로 옮겨 강열 회화한다. 그 후 상온이 될 때까지 식히고 황산 두 방울을 떨어뜨리고 다시 약 700 ℃로 2시간 가열한다. 상온이 될 때까지 식히고 잔류물의 질량을 정밀하게 재고 황산바륨(BaSO4)의 양으로 하여 몰농도계수를 계산하면 다음과 같아진다.
0.02 mol/L 염화바륨액 1 mL = 4.668 mg BaSO4
염화안티몬(III) SbCl3 [최순품]
염화안티몬(III)시액 클로로포름을 같은 용량의 물로 2 ∼ 3 회 씻은 다음 새로 강열하여 식힌 탄산칼륨을 넣어 마개를 하고 차광하여 하루밤 방치한다. 클로로포름층을 분취하여 되도록이면 차광하여 증류한다. 이 클로로포름으로 염화안티몬(III)의 표면을 씻어 씻은 액이 맑고 투명하게 된 후에 클로로포름을 넣어 포화용액으로 하여 차광하고 마개한 병에 넣는다. 쓸 때 만든다.
염화암모늄 NH4Cl [최순품]
염화암모늄시액 염화암모늄 10.5 g을 물에 녹여 100 mL로 한 용액으로 한다 (2 mol/L).
염화석(II)시액, 산성 염화석(II)이수화물 8 g을 염산 500 mL에 녹인 용액으로 만들어, 마개가 달린 병에 보관하고 조제후 3 개월 이내에 사용한다.
염화석(II)이수화물 SnCl2ㆍ2H2O [최순품]
염화수은(II) HgCl2 [최순품]
옥살산암모늄일수화물 (NH4)2C2O4ㆍH2O [최순품]
옥살산암모늄시액 옥살산암모늄일수화물 3.5 g에 물을 넣어 녹여 100 mL로 한다 (0.25 mol/L).
요오드화칼륨 KI [요오드화칼륨, 최순품]
요오드화칼륨시액 요오드화칼륨 16.5 g을 물에 녹여 100 mL로 한 것으로 하며, 차광하여 보관한다. 쓸 때 만든다.
요오드화칼륨ㆍ전분지(Potassium IodideㆍStarch Paper) 새로 만든 요오드화칼륨ㆍ전분시액에 여과지를 담그어 산 또는 알칼리의 증기가 없는 방에서 건조하여 만든다. 마개있는 병에 넣어 광선 및 습기가 없는 곳에서 보관한다.
용해아세틸렌 C2H2 [최순품]
왕수 염산 3 용량에 질산 1 용량을 넣는다. 쓸 때 만든다.
유리섬유 유리솜 참조.
유리솜 [최순품]
이소프로필에텔 (CH3)2CHOCH(CH3)2 무색의 맑은 액으로 특이한 냄새가 있으며, 물과 섞이지 않는다. 굴절율 : 1.368 ∼ 1.369, 비중 : 0.723 ∼ 0.725
이소프로필에텔, 추출용 이소프로필에텔 1 L를 수산화나트륨 용액(2.15 → 100) 100 mL로 두 번, 물 100 mL로 세 번 씻은 것으로 한다.
이크롬산칼륨 K2Cr2O7 [최순품]
이크롬산칼륨(표준시약) K2Cr2O7 [용량분석용표준물질]
1/60 mol/L 이크롬산칼륨액 1000 mL 중 이크롬산칼륨 (K2Cr2O7 : 294.18) 4.903 g을 함유한다.
조 제 이크롬산칼륨 (표준시약)을 가루로 하여 100 ∼ 110 ℃에서 3 ∼ 4 시간 건조한 다음 데시케이터 (실리카겔)에서 방랭하여 약 4.903 g을 정밀하게 달아 물을 넣어 녹여 정확하게 1000 mL로 하고 규정도계수를 계산한다.
인산수소이나트륨십이수화물 Na2HPO4ㆍ12H2O [최순품]
인산이수소칼륨 KH2PO4 [최순품]
인산완충액(pH 7.5)
제 1 액 : 인산수소이나트륨십수화물 53.7g을 물에 녹여 1,000mL로 한다.
제 2 액 : 인산이수소칼륨 20.4g을 물에 녹여 1,000mL로 한다.
제 1 액 21용량과 제 2 액 4용량을 섞고 양액을 사용하여 pH를 7.5로 한다.
등색 403 호 표준용액 박층크로마토그래프용 표준품 일람표 중의 등색 403 호 0.05 g을 클로로포름에 녹여 100 mL 용액으로 만든다.
자일레놀오렌지 C31H30N2Na2O13S [최순품]
자일레놀오렌지시액 자일레놀오렌지 100 mg에 물을 넣어 녹여 100 mL로 한다
전분시액 전분 1 g을 냉수 10 mL와 잘 섞고 이것을 열탕 200 mL 중에 계속하여 저으면서 천천히 넣고 액이 반투명하게 될 때까지 끓이고 용액을 방치한 다음 위의 맑은 액을 쓴다. 쓸 때 만든다.
질산 HNO3 [최순품, 비중 약 1.42] 69 % ∼ 70 %를 함유하는 것으로 한다.
질산납(II) Pb(NO3)2 [최순품]
질산마그네슘 Mg(NO3)2 [최순품]
질산마그네슘육수화물 Mg(NO3)2ㆍ6H2O [최순품]
질산, 묽은 질산 10.5 mL에 물을 넣어 100 mL 용액으로 한다 (10 %).
질산은 AgNO3 [최순품]
질산은시액 질산은 17.5 g을 물에 녹여 1 L 용액으로 만들고 (0.1 mol/L), 차광하여 보관한다.
0.1 mol/L 질산은액 1 L 중 질산은 (AgNO3 : 169.87) 16.987 g을 함유하는 용액으로 다음의 규정을 따른다.
1) 조제 : 질산은 17.0 g을 물에 녹여 1 L로 하여 다음과 같이 표정한다.
2) 표정 : 염화나트륨 (표준시약)을 500 ∼ 650 ℃로 40 ∼ 50 분간 건조한 후, 데시케이터 (실리카겔)안에 넣고 식히고, 그 중 약 0.15 g을 정밀하게 재어 물 50 mL에 녹이고 플루오레세인나트륨시액 세 방울을 떨어뜨리고 강하게 흔들어 섞으며 조제한 질산은액으로 액의 황록색이 황색에서 황등색을 띨 때까지 적정하여 계수를 계산한다.
0.1 mol/L 질산은액 1 mL = 5.844 mg NaCl
3) 저장법 : 차광하여 보존한다.
철표준액 황산암모늄철(III)십이수화물 86.3 mg을 정밀하게 달아 물 100 mL에 녹이고 묽은염산 5 mL와 물을 넣어 정확히 1 L 용액으로 만든다. 이 액 1 mL는 철(Fe) 0.01 mg를 함유한다.
철표준원액 (원자흡광광도법용) 황산암모늄철(III)십이수화물 8.634 g을 정밀하게 달아 물 100 mL에 녹이고 묽은염산 5 mL와 물을 넣어 정확히 1 L 용액으로 만든다.
칠몰리브덴산육암모늄사수화물 (NH4)6Mo7O24ㆍ4H2O [최순품]
쿠페론 C6H9N3O2 [쿠페론(니트로소페닐히드록실아민암모늄염), 최순품]
쿠페론시액 쿠페론 6 g에 물을 넣어 녹여 100 mL로 한다. 쓸 때 만든다.
크롬산칼륨 K2CrO4 [최순품]
크롬산칼륨시액 크롬산칼륨 10 g에 물을 넣어 녹여 100 mL 용액으로 만든다.
크롬표준원액 (원자흠광광도법용) 이크롬산칼륨(표준시약) 2.828 g을 정밀히 달아 물에 녹여 정확히 1 L 용액으로 만든다.
클로로포름 CHCl3 [최순품]
타르타르산나트륨칼륨사수화물 KNaC4H4O6ㆍ4H2O [(+)-주석산나트륨칼륨사수화물, 최순품]
타르타르산수소나트륨 타르타르산수소나트륨일수화물 참조.
타르타르산수소나트륨시액 타르타르산수소나트륨일수화물 1 g에 물을 넣어 녹여 10 mL로 한다 (0.5 mol/L). 쓸 때 만든다.
타르타르산수소나트륨일수화물 NaHC4H4O6ㆍH2O [최순품]
탄산나트륨 (표준시약) Na2CO3 [용량분석용표준물질]
탄산나트륨, 무수 Na2CO3 [탄산나트륨, 최순품]
탄산나트륨시액 무수탄산나트륨 10.5 g에 물을 넣어 녹여 100 mL로 한다 (2 mol/L).
탄산수소나트륨 NaHCO3 [최순품]
탄산칼륨 K2CO3 [최순품]
톨루엔 C6H5CH3 [최순품]
티오시안산수은암모늄시액 티오시안산암모늄 30 g 및 염화수은(II) 27 g에 물을 넣어 녹여 1000 mL로 한다.
티오시안산암모늄 NH4SCN [최순품]
티오시안산암모늄시액 티오시안산암모늄 8 g을 물에 녹여 100 mL 용액으로 만든다 (1 mol/L).
0.1 mol/L 티오시안산암모늄액 1 L중에 티오시안산암모늄(NH4SCN : 76.12) 7.612 g을 함유하는 용액으로 다음 규정에 따른다.
1) 조제 : 티오시안산암모늄 8 g을 물에 녹여 1 L로 하고 다음과 같이 표정한다.
2) 표정 : 0.1 mol/L 질산은액 25 mL를 정확하게 달아 물 50 mL, 질산 2 mL 및 황산암모늄철(III)시액 2 mL를 넣고 흔들면서 조제한 티오시안산암모늄액으로 적갈색을 지속적으로 띨 때까지 적정하여 계수를 계산한다.
3) 저장법 : 차광하여 보관한다.
티오우레아 H2NCSNH2 [최순품]
티오우레아시액 티오우레아 10 g에 물을 넣어 녹여 100 mL로 한다.
티오황산나트륨오수화물 Na2S2O3ㆍ5H2O [최순품]
0.1 mol/L 티오황산나트륨액 1000 mL 중 티오황산나트륨오수화물 (Na2S2O3ㆍ5H2O : 248.19) 24.819 g을 함유한다.
1) 조제 티오황산나트륨오수화물 25 g 및 무수탄산나트륨 0.2 g에 새로 끓여 식힌 물을 넣어 1000 mL로 하고 24 시간 방치하고 다음과 같이 표정한다.
2) 표정 요오드산칼륨 (표준시약)을 120 ∼ 140 ℃에서 1.5 ∼ 2 시간 말리고 데시케이터 (실리카겔)에서 방랭한 다음 약 0.1 g을 요오드병에 정밀하게 달아 물 25 mL를 넣어 녹인다. 여기에 요오드화칼륨 2 g 및 묽은황산 10 mL를 넣고 마개를 하여 10 분간 방치한 다음 물 100 mL를 넣어 유리된 요오드를 조제된 티오황산나트륨액으로 적정하여 규정도계수를 계산한다. 다만 적정의 종말점은 액이 종말점 부근에서 연한 노란색으로 되었을 때 전분시액 3 mL를 넣어 생긴 파란색이 탈색될 때로 한다. 같은 방법으로 공시험을 하여 보정한다.
0.1 mol/L 티오황산나트륨액 1 mL= 3.5667 mg KIO3
주의 : 오랫동안 보존한 것은 표정하여 보정한다.
트리에탄올아민 2,2',2″-니트릴트리에탄올 (CH2CH2OH)3N [순품]
파라니트로아닐린 박층크로마토그래프용 표준품과 같다.
파라니트로아닐린표준용액 파라니트로아닐린 1.0 g을 에탄올(95)에 녹여 100 mL 용액으로 만든다.
퍼옥시이황산암모늄 (NH4)2S2O8 [최순품]
페놀프탈레인 C20H14O4 [최순품]
페놀프탈레인시액 페놀프탈레인 1 g을 에탄올(95) 100 mL에 녹인 용액으로 만든다.
페리시안화칼륨 헥사시아노철(III)산칼륨 참조.
페리시안화칼륨시액 헥사시아노철(III)산칼륨시액 참조.
페리시안화칼륨시액 페리시안화칼륨 1 g을 물에 녹여 100 mL로 한다. 이 액 4mL를 취하여 수산화나트륨용액 ( 1 → 7 )을 넣어 100 mL로 한다. 이 약은 쓸 때 만든다. (푸르설티아민)
페로시안화칼륨 헥사시아노철(II)산칼륨삼수화물 참조.
페로시안화칼륨시액 헥사시아노철(II)산칼륨시액 참조.
포화수산암모늄용액 수산암모늄일수화물 5 g을 물 100 mL에 넣고 잘 흔들어 섞어 23 ∼ 27 ℃ 로 하고 충분히 포화시킨 후 그 온도에서 상층액을 여과하여 얻은 투명한 여액이다.
포화황산암모늄용액 황산암모늄 50 g을 달아 물 100 mL에 넣고 잘 흔들어 섞어 23 ∼ 27 ℃ 로 하고 충분히 포화시킨 후 그 온도에서 상층액을 여과하여 얻은 투명한 여액이다.
플라비안산 C10H6N2O8S 박층크로마토그래프용표준품과 같다.
플라비안산표준용액 플라비안산 0.01 g을 물에 녹여 10 mL 용액으로 만든다.
플루오레세인나트륨 C20H10Na2O5 [대한민국약전 의약품 각조, ‘플루오레세인나트륨’]
플루오레세인나트륨시액 플루오레세인나트륨 0.2 g을 물에 녹여 100 mL 용액으로 만든다.
피리딘 C5H5N [최순품]
pH측정용 사붕산나트륨십수화물 Na2B4O7ㆍ10H2O [사붕산나트륨십수화물, pH표준액용]
pH측정용 수산화칼슘 Ca(OH)2 [최순품] 23 ∼ 27 ℃로 얻은 포화용액의 25 ℃에서의 pH가 12.45인 용액을 쓴다.
pH측정용 이수산삼수소칼륨이수화물 KH3(C2O4)2ㆍ2H2O [이수산삼수소칼륨이수화물, pH측정용]
pH측정용 인산수소이나트륨 Na2HPO4 [인산수소이나트륨, pH표준액용]
pH측정용 인산이수소칼륨 KH2PO4 [인산이수소칼륨, pH표준액용]
pH측정용 탄산나트륨 Na2CO3 [pH표준액용]
pH측정용 탄산수소나트륨 NaHCO3 [pH표준액용]
pH측정용 프탈산수소칼륨 C6H4(COOK)(COOH) [pH표준액용]
헥사시아노철(II)산칼륨삼수화물 K4Fe(CN)6ㆍ3H2O [최순품]
헥사시아노철(II)산칼륨시액 헥사시아노철(II)산칼륨삼수화물 1 g을 물에 녹여 10 mL 용액으로 하고 (0.25 mol/L), 쓸 때 만든다.
활성탄 [대한민국약전 의약품 각조, ‘약용탄’]
황산 H2SO4 [최순품]
황산, 묽은 황산 5.7 mL를 물 10 mL에 주의하면서 넣고 상온이 될 때까지 냉각하고 물을 넣어 100 mL 용액으로 만든다.
0.5 mol/L 황산 1000 mL 중 황산(H2SO4 : 98.08) 49.04 g을 함유한다.
1) 조제 황산 30 mL를 물 1000 mL 중에 저어 섞으면서 천천히 넣어 방랭하고 다음과 같이 표정한다.
2) 표정 탄산나트륨 (표준시약)을 500 ∼ 650 ℃에서 40 ∼ 50 분간 가열한 다음 데시케이터 (실리카겔)에서 방랭하고 약 1.3 g을 정밀하게 달아 물 50 mL를 넣어 녹여 메틸레드시액 3 방울을 넣고 조제된 황산으로 적정하여 규정도계수를 계산한다. 다만 적정의 종말점은 액을 조심하여 끓여서 가볍게 마개를 하고 식힐 때 지속적인 주황색 ∼ 등적색을 나타낼 때로 한다.
0.5 mol/L 황산 1 mL = 52.99 mg Na2CO3
0.05 mol/L 황산 1 L중 황산 (H2SO4:98.08) 4.904 g을 포함하는 것으로 다음의 규정에 따른다.
1) 조제 : 황산 3 mL를 물 1 L에 흔들어 섞으면서 천천히 넣고 다음과 같이 표정 한다.
2) 표정 : 탄산나트륨 (표준시약)을 500 ∼ 650 ℃로 40 ∼ 50 분간 가열하고 데시케이터 (실리카겔)에서 식힌 다음 그 중 약 0.15 g을 정밀하게 달아 물 30 mL에 녹이고 메틸레드시액 3 방울을 넣고 조제한 황산으로 적정하여 계수를 계산한다. 단 적정의 종말점은 액을 주의해서 가열하여 느슨하게 마개를 한 상태로 냉각할 때 주황색 ∼ 적색의 일정의 색이 지속적으로 나타낼 때로 한다.
0.05 mol/L 황산 1 mL=5.299 mg Na2CO3
0.005 mol/L 황산 1 L 중 황산 (H2SO4:98.08) 0.4904 g을 함유하는 용액으로 만들고, 사용 시 0.05 mol/L 황산에 물을 넣어 정확히 10배 용량으로 한다.
0.001 mol/L 황산 1 L 중 황산 (H2SO4:98.08) 0.098 g을 함유하는 용액으로 만들고, 사용 시 0.05 mol/L 황산에 물을 넣어 정확히 50 배 용량으로 한다.
황산구리(Ⅱ)오수화물 CuSO4ㆍ5H2O [최순품]
황화나트륨구수화물 Na2Sㆍ9H2O [최순품]
황화나트륨시액 황화나트륨구수화물 5 g을 물 10 mL과 글리세린 30 mL의 혼합액에 녹인 것으로한다. 또는, 수산화나트륨 5 g을 물 30 mL과 글리세린 90 mL의 혼합액에 녹여 그 반 용량에 차가운 황화수소를 포화시키고 여기에 나머지의 반 용량을 합한 것으로 한다. 차광한 병에 거의 가득 채워 보존하며, 조제 후 3개월 이내에 사용한다.
황산마그네슘시액 황산마그네슘칠수화물 12 g에 물을 넣어 녹여 100 mL로 한다 (0.5 mol/L).
황산마그네슘칠수화물 MgSO4ㆍ7H2O [최순품]
황산암모늄 (NH4)2SO4 [최순품]
황산암모늄철(Ⅲ)시액 황산암모늄철(Ⅲ)십이수화물 14 g을 물 100 mL에 넣어 잘 흔들어 섞으면서 녹이고 여과한 후 황산 10 mL를 넣은 용액으로 한다.
황산암모늄철(Ⅲ)십이수화물 FeNH4(SO4)2・12H2O [황산암모늄철(Ⅲ)・12물, 최순품]
헥사니트로코발트(III)산나트륨 Na3Co(NO2)6 [최순품]
헥사니트로코발트(III)산나트륨시액 헥사니트로코발트(III)산나트륨 10 g에 물을 넣어 녹여 50 mL로 하고 필요하면 여과한다. 쓸 때 만든다.
헥사시아노철(III)산칼륨 K3Fe(CN)6 [최순품]
헥사시아노철(III)산칼륨시액 헥사시아노철(III)산칼륨 1 g에 물을 넣어 녹여 10 mL로 한다. 쓸 때 만든다 (0.3 mol/L).
2) 박층크로마토그래프용표준품
1. 다음의 표준품
적색 2 호 표준품
적색 102 호 표준품
적색 103 호의 (1) 표준품
적색 104 호의 (1) 표준품
적색 104 호의 (2) 표준품
적색 106 호 표준품
황색 4 호 표준품
황색 5 호 표준품
녹색 3 호 표준품
청색 1 호 표준품
청색 2 호 표준품
적색 202 호 표준품
적색 218 호 표준품
적색 221 호 표준품
적색 223 호 표준품
적색 230 호의 (2) 표준품
등색 205 호 표준품
황색 201 호 표준품
적색 504 호 표준품
적색 506 호 표준품
황색 401 호 표준품
황색 403 호의 (1) 표준품
2. 파라니트로아닐린 C6H6N2O2 [p-니트로아닐린. 최순품] 파라니트로아닐린을 다음의 정제법으로 박층크로마토그래프용으로 정제한 것으로 다음 규격에 적합하여야 한다.
정제법 : 파라니트로아닐린 10 g에 에탄올(95) 100 mL를 넣고 가온하여 녹인 후 따뜻한 상태에서 여과하여 여액을 실온에서 5 시간 정도 그대로 둔다. 석출한 결정을 여과하여 얻고 바람에 건조하고 데시케이터 (감압, 실리카겔)에서 두 시간 동안 건조한다.
성상 : 황색의 침상 결정으로 냄새는 거의 없다.
융점 : 147 ∼ 150 ℃
3. 플라비안산 황색 403 호의 (1) 표준품 0.1 g에 물 2 mL를 넣어 녹인 후 염산 50 μL를 넣고 잘 섞어 약 5 ℃에서 한 시간 정도 그대로 둔다. 석출한 결정을 여과해 얻어 바람에 건조하고 데시케이터 (감압, 실리카겔)에서 두 시간 건조한 것으로 황색의 침상 결정으로 냄새는 거의 없고 다음 순도시험에 적합하다.
순도시험 : 이 약의 수용액(1 → 1000) 2 μL를 1-부탄올ㆍ에탄올(95)ㆍ묽은암모니아시액혼합액(6 : 2 : 3)을 전개용매로 하여 박층크로마토그래프법 제 1 법에 따라 시험할 때, Rf값 0.6 부근의 황색 주반점 외에 반점은 나타나지 않는다.
3) 계량기ㆍ용기
온 도 계 일반적으로 침선부온도계 (봉상) 또는 전몰식수은온도계 (봉상)를 기차(器差)시험을 한 다음에 쓴다. 다만, 융점측정법은 침선부온도계 (봉상)를 쓴다. 표 1.
화학용체적계 용량플라스크, 피펫, 뷰렛 및 메스실린더는 한국산업규격에 적합한 것을 쓴다.
네슬러관 무색, 두께 1.0 ∼ 1.5 mm의 갈아 맞춘 유리 마개가 있는 경질유리원통으로 그림에 표시한 것과 같다. 다만, 각각의 관의 50 mL 눈금선 높이의 차이가 2 mm 이하인 것을 쓴다.
천칭 및 분동
1) 화학천칭 0.1 mg까지 칭량할 수 있는 것을 쓴다.
2) 세미마이크로천칭 0.01 mg까지 칭량할 수 있는 것을 쓴다.
3) 마이크로천칭 0.001 mg까지 칭량할 수 있는 것을 쓴다.
4) 분동 검정한 것을 쓴다.
유리여과기 한국산업규격에 적합한 것을 쓴다.
체 다음에 표 2에 표시한 규격의 것을 쓴다. 각각의 이름은 체번호 또는 호칭치수(μm)로 한다.
여지 다음과 같은 것을 쓴다. 또한 여지로 기재하고 구체적인 종류를 표시하지 않은 것은 정성분석용여지를 쓴다.
1) 정성분석용여지 한국산업규격의 여지 (화학분석용)의 정성분석용 규격에 적합한 것을 사용한다.
2) 정량분석용여지 한국산업규격의 여지 (화학분석용)의 정량분석용 규격에 적합한 것을 사용한다.
표 1. 온도계
| 1호 | 2호 | 3호 | 4호 | 5호 | 6호 |
액 체 액상(液上)에 채운 기체 온 도 범 위 (℃) 최 소 눈 금 (℃) 긴 눈금의 선 눈 금 의 숫 자 길 이 (mm) 아래몸체의 지름 (mm) 수은구의 길이 (mm) 수은구 하단에서 최저눈금선까지의 거리 (mm) 온도계 상단에서 최고 눈금선까지의 거리 (mm) 수은구 하단에서 침선까지의 거리 (mm) 꼭 지 모 양 허 용 오 차 | 수 은 질 소 -17 ∼ 50 0.2 1 ℃ 마다 2 ℃ 마다 280 ∼ 300 6.0 ± 0.1 12 ∼ 15 75 ∼ 90 35 ∼ 50 60 환 상 0.2 ℃ | 수 은 질 소 40 ∼ 100 0.2 1℃ 마다 2℃ 마다 280 ∼ 300 6.0 ± 0.1 12 ∼ 15 75 ∼ 90 35 ∼ 50 60 환 상 0.2 ℃ | 수 은 질 소 90 ∼ 150 0.2 1℃ 마다 2℃ 마다 280 ∼ 300 6.0 ± 0.1 12 ∼ 15 75 ∼ 90 35 ∼ 50 60 환 상 0.2 ℃ | 수 은 질 소 140 ∼ 200 0.2 1℃ 마다 2℃ 마다 280 ∼ 300 6.0 ± 0.1 12 ∼ 15 75 ∼ 90 35 ∼ 50 60 환 상 0.2 ℃ | 수 은 질 소 190 ∼ 250 0.2 1℃ 마다 2℃ 마다 280 ∼ 300 6.0 ± 0.1 12 ∼ 15 75 ∼ 90 35 ∼ 50 60 환 상 0.2 ℃ | 수 은 질 소 240 ∼ 320 0.2 1℃ 마다 2℃ 마다 280 ∼ 300 6.0 ± 0.1 12 ∼ 15 75 ∼ 90 35 ∼ 50 60 환 상 0.4 ℃ |
그림. 네슬러관의 예
표 2. 체의 규격
체 번호 | 호칭 눈 크기 (μm) | 체의 규격 | |||||
체눈의 크기 | 선재 | ||||||
치수(mm) | 허용차 | 선지름(mm) | 선지름의 허용범위 | ||||
평균(±X) | 최대(+Y) | 최대선지름 | 최소선지름 | ||||
3.5 | 5600 | 5.6 | 0.18 | 0.47 | 1.6 | 1.9 | 1.3 |
4 | 4750 | 4.47 | 0.15 | 0.41 | 1.6 | 1.9 | 1.3 |
4.7 | 4000 | 4 | 0.13 | 0.37 | 1.4 | 1.7 | 1.2 |
5.5 | 3350 | 3.35 | 0.11 | 0.32 | 1.25 | 1.5 | 1.06 |
6.5 | 2800 | 2.8 | 0.09 | 0.29 | 1.12 | 1.3 | 0.95 |
7.5 | 2360 | 2.36 | 0.08 | 0.25 | 1 | 1.15 | 0.85 |
8.6 | 2000 | 2 | 0.07 | 0.23 | 0.9 | 1.04 | 0.77 |
10 | 1700 | 1.7 | 0.06 | 0.2 | 0.8 | 0.92 | 0.68 |
12 | 1400 | 1.4 | 0.05 | 0.18 | 0.71 | 0.82 | 0.6 |
14 | 1180 | 1.18 | 0.04 | 0.16 | 0.63 | 0.72 | 0.54 |
16 | 1000 | 1 | 0.03 | 0.14 | 0.56 | 0.64 | 0.48 |
18 | 850 | 0.85 | 0.029 | 0.127 | 0.5 | 0.58 | 0.43 |
22 | 710 | 0.71 | 0.025 | 0.112 | 0.45 | 0.52 | 0.38 |
26 | 600 | 0.6 | 0.021 | 0.101 | 0.4 | 0.46 | 0.34 |
30 | 500 | 0.5 | 0.018 | 0.089 | 0.315 | 0.36 | 0.27 |
36 | 425 | 0.425 | 0.016 | 0.081 | 0.280 | 0.32 | 0.24 |
42 | 355 | 0.355 | 0.013 | 0.072 | 0.224 | 0.26 | 0.19 |
50 | 300 | 0.3 | 0.012 | 0.065 | 0.200 | 0.23 | 0.17 |
60 | 250 | 0.25 | 0.0099 | 0.058 | 0.16 | 0.19 | 0.13 |
70 | 212 | 0.212 | 0.0087 | 0.052 | 0.14 | 0.17 | 0.12 |
83 | 180 | 0.18 | 0.0076 | 0.047 | 0.125 | 0.15 | 0.106 |
100 | 150 | 0.15 | 0.0066 | 0.043 | 0.1 | 0.115 | 0.085 |
119 | 125 | 0.125 | 0.0058 | 0.038 | 0.09 | 0.104 | 0.077 |
140 | 106 | 0.106 | 0.0052 | 0.035 | 0.071 | 0.082 | 0.060 |
166 | 90 | 0.09 | 0.0046 | 0.032 | 0.063 | 0.072 | 0.054 |
200 | 75 | 0.075 | 0.0041 | 0.029 | 0.050 | 0.058 | 0.043 |
235 | 63 | 0.063 | 0.0037 | 0.026 | 0.045 | 0.052 | 0.038 |
282 | 53 | 0.053 | 0.0034 | 0.024 | 0.036 | 0.041 | 0.031 |
330 | 45 | 0.045 | 0.0031 | 0.022 | 0.032 | 0.037 | 0.027 |
391 | 38 | 0.038 | 0.0029 | 0.02 | 0.030 | 0.035 | 0.024 |









